
科目: 来源: 题型:选择题
| A. | Cu(OH)2溶于醋酸:Cu(OH)2+2H+═Cu2++2H2O | |
| B. | NH4HCO3溶液与足量KOH浓溶液共热:N${H}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | NaHSO4溶液与NaOH溶液混合:OH-+H+═H2O | |
| D. | 明矾溶液中加入过量Ba(OH)2溶液:2Al3++3S${O}_{4}^{2-}$+3Ba2++8OH-═2Al${O}_{2}^{-}$+3BaSO4↓+4H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 相关物质 | 相关说法 |
| A | 1mol CH3COONa和少量CH3COOH溶于水所得的中性溶液中 | CH3COO-数目为NA |
| B | Na2O和Na2O2的混合物共1mol | 阴离子数目可能为1.5NA |
| C | 向含2mol H2SO4的浓硫酸中加入足量的Zn粉,加热充分反应 | 转移的电子数为2NA |
| D | 3.0g由淀粉和葡萄糖组成的混合物中 | 所含的碳原子数为0.1NA |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氧化硅能与氢氟酸反应,可用于制光导纤维 | |
| B. | 氧化铝熔点很高,可用于制耐火材料 | |
| C. | 新制氢氧化铜悬浊液具有碱性,可用于检验醛基 | |
| D. | 浓硫酸具有脱水性,可用于干燥氯气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:Na+、Fe2+、SO42-、MnO4- | |
| B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:K+、Na+、Cl-、HCO3- | |
| C. | 0.1 mol•L-1的NH4I溶液中:Mg2+、Na+、ClO-、NO3- | |
| D. | 0.1 mol•L-1的CuSO4溶液中:Mg2+、Al3+、Br-、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢氧化钠的电子式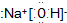 | |
| B. | 质子数为29、中子数为35的铜原子${:}_{29}^{35}$Cu | |
| C. | 氯离子的结构示意图: | |
| D. | 对苯二酚的结构简式: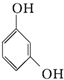 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲醇是弱电解质 | B. | 所有烯烃都符合通式CnH2n | ||
| C. | 丙烯可发生加聚反应生成聚丙烯 | D. | 煤干馏可得到甲醇 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Si是一种非金属主族元素,其晶体可用于制作计算机芯片 | |
| B. | 光导纤维和石英玻璃主要成分都是二氧化硅 | |
| C. | 过量CO2通入Na2SiO3溶液,最终无沉淀产生 | |
| D. | 硅胶疏松多孔,可用作催化剂的载体 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com