
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应BaSO4(s)+4C(s)═BaS(s)+4CO(g)在室温下不能自发进行,说明该反应的△H<0 | |
| B. | 已知室温时氢氧化铁的溶度积常数为2.6×10-39,为除去某酸性CuCl2溶液中少量的氯化铁,可加入适量碱式碳酸铜调节溶液的pH到4,使Fe3+转化为氢氧化铁沉淀,此时溶液中的c(Fe3+)为2.6×10-8 mol/L | |
| C. | 相同物质的量浓度的下列溶液:①NH4Al(SO4)2②NH4Cl ③NH3•H2O,c(NH4+)由大到小的顺序是:①>②>③ | |
| D. | 向Cu(OH)2悬浊液中加入胆矾,则平衡左移,氢氧化铜的溶解度不变 |
查看答案和解析>>
科目: 来源: 题型:多选题
| 序号 | 实验内容 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去 | 证明Na2CO3溶液中存在水解平衡 |
| B | 将Al泊插入浓硝酸中,无现象 | 证明Al和浓硝酸不反应 |
| C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对化学平衡状态的影响 |
| D | 向同体积同浓度的H2O2溶液中,分别加入1mL同浓度的CuSO4、FeCl3溶液 | 比较Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  的命名为:2-甲基-1-丙醇 的命名为:2-甲基-1-丙醇 | |
| B. | 有机物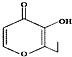 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 | |
| C. | 布洛芬结构如图所示 该物质可发生氧化、还原、加成、消去、取代反应 该物质可发生氧化、还原、加成、消去、取代反应 | |
| D. | 经测定乙二醇和苯组成的混合物中氧的质量分数为8%,则此混合物中碳的质量分数是84% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素B、C、D的简单氢化物中化学键类型相同 | |
| B. | 原子半径A>B>C>D>E | |
| C. | 由元素A、E形成的单质晶体类型相同 | |
| D. | AB形成的化合物中只可能含离子键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | “辽宁舰”上用于舰载机降落拦阻索的是一种特种钢缆,属于新型无机非金属材料 | |
| B. | 新型氢动力计程车的投入使用有益于减少雾霾的产生 | |
| C. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 | |
| D. | 生物柴油是由动植物油脂与甲醇或乙醇,在酸或碱的催化及高温下进行反应,或在温和的条件下,用酶催化反应,生成的高级脂肪酸甲酯或乙酯 |
查看答案和解析>>
科目: 来源: 题型:解答题
 在一密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系图,回答下列问题:
在一密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系图,回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
 用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com