
科目: 来源: 题型:选择题
| A. | 2mol/l | B. | 4mol/l | C. | 1 mol/l | D. | 20mol/l |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| B. | 用可见光束照射以区别溶液和胶体 | |
| C. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| D. | H+、K+、S2-、Br-能在Fe(OH)3胶体中大量共存 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,在该反应中,当有3NA电子转移时,上述热化学反应方程式的焓变为△H=-46.2KJ/mol | |
| B. | 1L 0.1mol•L-1碳酸钠溶液的阴离子总数等于0.1NA | |
| C. | 室温下pH=13的NaOH溶液中含有的OH-0.1NA | |
| D. | 浓度分别为1mol•L-1和0.5mol•L-1的CH3COOH和CH3COONa混合液共1L,含CH3COOH和CH3COO-共1.5mol |
查看答案和解析>>
科目: 来源: 题型:解答题
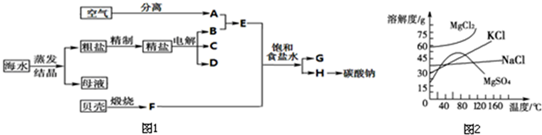
查看答案和解析>>
科目: 来源: 题型:解答题
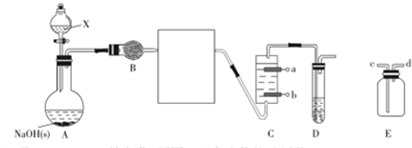
查看答案和解析>>
科目: 来源: 题型:解答题
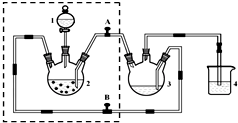 醋酸亚铬水合物{[Cr(CH3COO)2)]2•2H2O,深红色晶体}是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,易溶于乙醇和盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物{[Cr(CH3COO)2)]2•2H2O,深红色晶体}是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,易溶于乙醇和盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:查看答案和解析>>
科目: 来源: 题型:解答题
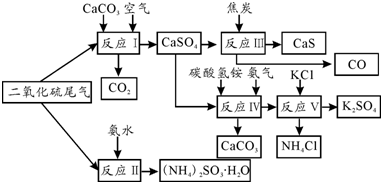
查看答案和解析>>
科目: 来源: 题型:解答题
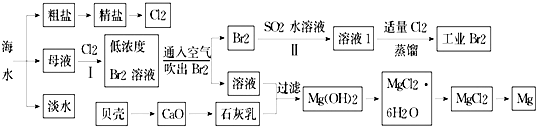
查看答案和解析>>
科目: 来源: 题型:解答题
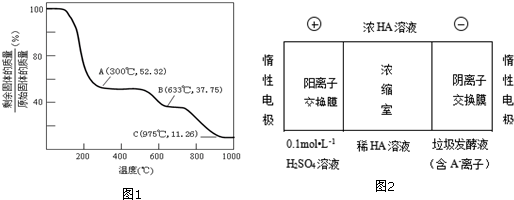
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com