
科目: 来源: 题型:选择题
| A. | 表示物质微粒个数的物理量 | B. | 表示物质微粒集体的物理量 | ||
| C. | 表示物质质量的物理量 | D. | 表示物质的质量和个数的物理量 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2O2投入水中:2Na2O2+2H2O=4Na++4OH-+H2↑ | |
| B. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- | |
| C. | 钠投入CuSO4溶液中:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑ | |
| D. | 铜和稀HNO3反应:3Cu+8H++2NO3-=3Cu2++2NO2↑+4H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 用CH3 COOH溶解CaC03:CaCO3+2H+═Ca++H2O+CO2↑ | |
| C. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4↓+AlO${\;}_{2}^{-}$+2H2O | |
| D. | 用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
 、Na
、Na 、K+K+、OH-
、K+K+、OH- 、Na2O2
、Na2O2 、NH4Cl
、NH4Cl
 、NaCl:
、NaCl: .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X原子的电子层比Y原子的电子层数多 | |
| B. | X原子的最外层电子比Y原子的最外层电子多 | |
| C. | X的单质能将Y从NaY的溶液中置换出来 | |
| D. | Y的单质能将X从NaX的溶液中置换出来 |
查看答案和解析>>
科目: 来源: 题型:解答题
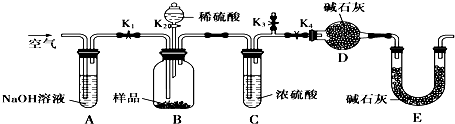
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com