
科目: 来源: 题型:选择题
| A. | 用电解法制取Na、Mg、Al | |
| B. | 电解熔融NaCl制Cl2 | |
| C. | 以硫或硫铁矿为原料通过接触法制硫酸 | |
| D. | 制硅:SiO2$→_{高温}^{C}$粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$高纯硅 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 某元素原子的原子半径是111pm | |
| B. | 某常见气体的密度为1.8g•cm-3 | |
| C. | 某澄清石灰水的浓度是2.0mol•L-1 | |
| D. | 用广泛pH试纸测得某溶液的pH为6.3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
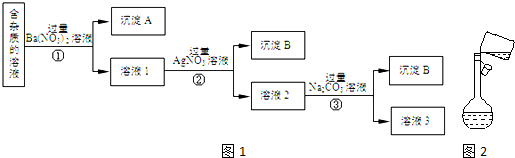
| A. | 肯定不存在的离子是Fe3+、Cu2+、CO32-、Br- | |
| B. | 肯定存在的离子是K+、SO42-、SO32- | |
| C. | 无法确定原溶液中是否存在Cl-和CO32- | |
| D. | 若步骤④改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断也无影响 |
查看答案和解析>>
科目: 来源: 题型:选择题
 把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,再往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( )
把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,再往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( )| A. | HCl溶液的体积为80mL | B. | a的取值范围为0≤a<50 | ||
| C. | 当a值为30时,b值为0.01 | D. | $\frac{n(Mg)}{n(Al)}$的最大值为2.5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL | |
| B. | 当金属全部溶解时收集到NO气体的体积为4.48L(标准状况下) | |
| C. | 参加反应的金属的总质量一定是9.9g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 物质的量浓度相等的碳酸氢钡溶液和氢氧化钠溶液等体积混合Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O | |
| B. | NaHSO4溶液中滴加入Ba(OH)2溶液至中性:2H++Ba2++2OH-+SO42-=BaSO4↓+2H2O | |
| C. | 以石墨作电极电解氯化镁溶液:2Cl-+2H2O═2OH-+H2↑+Cl2↑ | |
| D. | 碳酸氢钠溶液加入氯化铝溶液 3HCO3-+Al3+?3CO2↑+Al(OH)3↓ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com