
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | BaCl2、Ba(NO3)2、NaCl | B. | Ba(NO3)2、KCl、MgCl2 | ||
| C. | Na2CO3、BaCl2、MgCl2 | D. | Na2CO3、K2CO3、NaCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4 L CO2含有2NA个氧原子 | |
| B. | 1 mol•L-1 NaOH溶液中含有NA个Na+ | |
| C. | 标准状况下,22.4L CCl4中含有NA个CCl4分子 | |
| D. | 常温常压下,28g氮气所占的体积为22.4 L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、HCl | ||
| C. | BaCl2、Na2CO3、HNO3 | D. | BaCl2、K2CO3、HNO3 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,11.2L CO2所含的原子数为1.5NA | |
| B. | 常温常压下,48g O2含有的氧原子数为3NA | |
| C. | 标准状况下,22.4L H2中所含原子数为NA | |
| D. | 标准状况下,22.4L 四氯化碳的分子数为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 蒸发使用的主要仪器是蒸发皿、酒精灯、玻璃棒、带铁圈的铁架台 | |
| B. | 分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 | |
| C. | 丁达尔效应可以鉴别胶体和溶液 | |
| D. | 用规格为10 mL的量筒量取6.20 mL的液体 |
查看答案和解析>>
科目: 来源: 题型:解答题
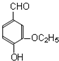 )是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
)是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com