
科目: 来源: 题型:解答题
 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应为CO(g)+2H2(g)═CH3OH(g)△H<0.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将PH=a的NaOH溶液加水稀释至10n倍,则溶液的PH变为a-n | |
| B. | 等浓度的氨水和NH4Cl溶液等体积混合后:c(NH${\;}_{4}^{+}$)+c(H+)>c(NH3•H2O)+c(OH-) | |
| C. | 向NaOH溶液中逐滴加入CH3COOH溶液至PH=7,水的电离程度逐渐增大 | |
| D. | PH=5.6的NaHSO3溶液:c(Na+)>c(HSO${\;}_{3}^{_}$)>c(H2SO3)>c(SO${\;}_{3}^{2-}$) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | n1=n2 | B. | n1>n2 | C. | n1<n2 | D. | c(A-)<c(B-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K=$\frac{c(C{O}_{3}^{2-})c({H}^{+})}{c({H}_{2}C{O}_{3})}$ | B. | K=$\frac{c(C{O}_{3}^{2-}){c}^{2}({H}^{+})}{c({H}_{2}C{O}_{3})}$ | ||
| C. | K1=$\frac{c(HC{O}_{3}^{-})c({H}^{+})}{c({H}_{2}C{O}_{3})}$ | D. | K2=$\frac{(C{O}_{3}^{2-})c({H}^{+})}{c(HC{O}_{3}^{-})}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ca(ClO)2+2HCl═CaCl2+2HClO | B. | Ca(ClO)2+2H2O+2CO2═Ca(HCO3)2+2H2O | ||
| C. | NaClO+H2O+CO2═NaHCO3+HClO | D. | Na2CO3+2HClO═2NaClO+H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:多选题
 在1.0L恒容密闭容器中投入1mol CO2和2.75mol H2发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示.下列说法不正确的是( )
在1.0L恒容密闭容器中投入1mol CO2和2.75mol H2发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示.下列说法不正确的是( )| A. | 该反应的正反应为放热反应 | |
| B. | 压强大小关系为p1<p2<p3 | |
| C. | M点对应的平衡常数K的值约为1.04×10-2 | |
| D. | 在p2及512K时,图中N点v(正)<v(逆) |
查看答案和解析>>
科目: 来源: 题型:解答题
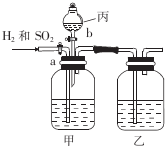 为了分离H2和SO2,并分别得到干燥的气体,某学生设计了一个实验装置.(a、b为活塞,且每个装置中的溶液均过量)
为了分离H2和SO2,并分别得到干燥的气体,某学生设计了一个实验装置.(a、b为活塞,且每个装置中的溶液均过量)查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 沉淀a的主要成分是BaS04和BaC03 | |
| B. | 滤液b中Na+的物质的量为0.08 mol | |
| C. | 气体d在标准状况下的体积为224 mL | |
| D. | 原混合物中Na2S04与Na2C03的物质的量之比为1:3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 100 ml. | B. | 250 ml. | C. | 500 ml. | D. | 1 L. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分液时,上层液体应从分液漏斗的上口倒出 | |
| B. | 蒸发时,应把蒸发皿中的水蒸干,再熄灭酒精灯 | |
| C. | 稀释时,把水倒人浓硫酸中 | |
| D. | 过滤时,为了加快过滤速度,可用玻璃棒搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com