
科目: 来源: 题型:解答题

| 空石英管质量 m0/g | 石英管与钙的质量 m1/g | 石英管与产物的质量 m2/g |
| 14.800 | 15.080 | 15.150 |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

| 温度 | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
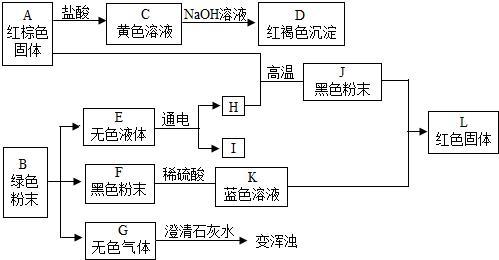
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe+2HCl═H2↑+FeCl2 | B. | 2FeCl2+Cl2 ═2FeCl3 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2Fe(OH)3 $\frac{\underline{\;△\;}}{\;}$Fe2O3+3H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CuSO4 •5H2O 是混合物 | |
| B. | 含Fe元素质量分数为70%的Fe2O3是纯净物 | |
| C. | 冰和水混合在一起形成混合物 | |
| D. | 由单质形成的物质一定是纯净物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 从组成上来说,Na2SO4 是钠盐、硫酸盐、正盐 | |
| B. | 氧化物不是碱性氧化物就是酸性氧化物 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 不含杂质的盐酸是纯净物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4m mol | B. | 10m mol | C. | $\frac{10m}{3}$mol | D. | $\frac{2m}{3}$mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等浓度的溶液中滴入稀盐酸.放出气体的快慢Na2C03<NaC03 | |
| B. | 热稳定性Na2C03<NaHC03 | |
| C. | 常温时水溶性Na2C03<NaHC03 | |
| D. | 相对分子质量Na2C03<NaHC03 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com