
科目: 来源: 题型:选择题
| A. | 用蒸发皿加热NaCl溶液 | |
| B. | 不慎将汞滴落到桌面上,应立即用较多的水冲洗 | |
| C. | 从试剂瓶中取出的一些Na2CO3溶液放入试管中,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| D. | 用瓷坩埚熔化氢氧化钠 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色 | |
| B. | 甲苯与浓硫酸和浓硝酸混酸反应生成2,4,6-三硝基甲苯 | |
| C. | 1mol甲苯能与3mol氢气发生加成反应 | |
| D. | 甲苯可以燃烧并产生浓烈的黑烟 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 烷烃不能发生加成反应,烯烃不能发生取代反应 | |
| B. | 烷烃中含饱和键、烯烃、炔烃中含不饱和键 | |
| C. | 能发生加成反应的一定是烯烃 | |
| D. | 符合通式CnH2n+2的一定是烷烃,符合通式CnH2n的一定是烯烃. |
查看答案和解析>>
科目: 来源: 题型:解答题
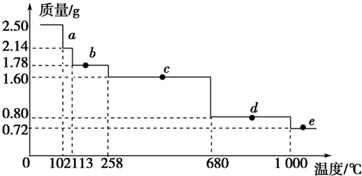
查看答案和解析>>
科目: 来源: 题型:解答题
 .
. +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O.
+2H2O. +2nNaOH$→_{△}^{NaOH溶液}$n
+2nNaOH$→_{△}^{NaOH溶液}$n +n
+n .
. (或
(或 等)(只写出一种即可).
等)(只写出一种即可).查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
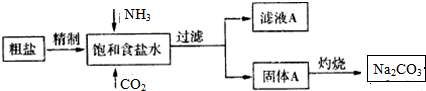
| A. | ①中的离子反应方程式是:Na++NH3+CO2+H2O=NaHCO3↓+NH4+ | |
| B. | ②中的离子反应方程式是:2Na++CO32-+H2O+CO2=2NaHCO3↓ | |
| C. | 上述变化说明相同温度下溶解度Na2CO3>NaHCO3>NaCl | |
| D. | 向饱和CaCl2溶液中加入浓Ba(OH)2溶液,也会析出晶体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硫酸氢钠溶于水既有离子键被破坏又有共价键被破坏 | |
| B. | 单质分子中均含共价键 | |
| C. | HF与HBr相比,分子内共价键更强,所以HF沸点更高 | |
| D. | 由不同元素组成的多原子分子里,只存在极性键 |
查看答案和解析>>
科目: 来源: 题型:解答题
 不变 D.溶液中
不变 D.溶液中 减小
减小| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com