
科目: 来源: 题型:选择题
| A. | 将混合气体通过盛有酸性KMnO4溶液的洗气瓶 | |
| B. | 将混合气体通过盛有适量溴水的洗气瓶 | |
| C. | 将混合气体中通入氢气,在Ni催化加热的条件下反应 | |
| D. | 将混合气体通过盛有NaOH溶液的洗气瓶 |
查看答案和解析>>
科目: 来源: 题型:解答题
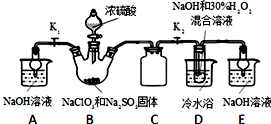
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 明矾是常用的净水剂、具有杀菌、消毒的作用 | |
| B. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| C. | 考古时,利用14C测定一些文物的年代 | |
| D. | 煤的干馏和石油的分馏都是化学变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用NaOH溶液滴定盐酸,滴定前尖嘴下端有气泡,滴定后气泡消失,会使结果偏高 | |
| B. | 仰视量筒刻度量取一定量浓硫酸所配制的0.10 mol•L-1 H2SO4溶液的浓度结果偏低 | |
| C. | 焰色反应实验中,铂丝在蘸取待测溶液前应先用稀硫酸洗净并灼烧至无色 | |
| D. | 要将溶解在CCl4中的碘分离出来,以用蒸馏法,因为碘易升华,先分离出来 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | OH-+H+═H2O | B. | OH-+CO32-+2H+═HCO3-+H2O | ||
| C. | OH-+CO32-+3H+═CO2↑+2H2O | D. | 2OH-+CO32-+4H+═CO2↑+3H2O |
查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 | |
| B. | 浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 | |
| C. | K2FeO4具有还原性,可用于自来水的杀菌消毒 | |
| D. | SO2具有漂白性,能使紫色KMnO4溶液褪色 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
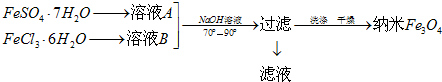
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com