
科目: 来源: 题型:选择题
| A. | 金属钠和水反应 2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 将四氧化三铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将过量铁粉和稀硝酸混合:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA | |
| B. | 标准状况下,14 g氮气含有的核外电子数为5NA | |
| C. | 标准状况下,5.6 L四氯化碳(CCl4)含有的分子数为0.25NA | |
| D. | NA个一氧化碳分子和0.5 mol 甲烷的质量比为7:4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 直接用酒精灯的外焰加热蒸发皿 | |
| B. | 加热过程中不断用玻璃棒搅拌 | |
| C. | 加热到液体全部消失 | |
| D. | 蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 烧杯、酒精灯、试管、铁架台(铁圈)、漏斗 | |
| B. | 烧杯、漏斗、玻璃棒、铁架台(铁圈)、滤纸 | |
| C. | 滤纸、烧杯、试管夹、漏斗、玻璃棒 | |
| D. | 滤纸、试管、漏斗、铁架台(铁圈)、玻璃棒 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,1molH2O的体积约为22.4L | |
| B. | 1mol/L的CaCl2溶液中含Cl-的数目为2 NA | |
| C. | 常温常压下,17g NH3含氢原子数目为3NA | |
| D. | 标准状况下,2.24 LCl2做成的氯水中含有0.1NA个Cl2分子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将溴乙烷滴入AgNO3溶液中,立即有淡黄色沉淀生成 | |
| B. | 溴乙烷与NaOH的水溶液共热可制取乙烯 | |
| C. | 溴乙烷难溶于水,能溶于多种有机溶剂 | |
| D. | 实验室通常用乙烯与溴水反应来制取溴乙烷 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ |
| 物质鉴定试验 | 推导结论 |
| ①用pH试纸测出A、B溶液呈碱性,C、D、E溶液呈酸性 | A、B中含有的阴离子为CO32-、OH-,C、D、E中含有的阳离子为H+、Al3+、Ag+ |
| ②A溶液与E溶液反应,既有气体产生又有沉淀产生,A与C反应只有气体产生 | A为Na2CO3,C含H+ |
| ③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀 | D为AgNO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | |
| B. | 质子数为92、中子数为146的U原子:${\;}_{92}^{146}$U | |
| C. | CH2F2的电子式: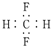 | |
| D. | Cl-的结构示意图: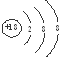 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com