
科目: 来源: 题型:选择题
| A. | 增大 | B. | 减小 | ||
| C. | 不变 | D. | 可能增大也可能减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 化学键 | H-H | C-O | C O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
| A. | 99、-41 | B. | +99、+41 | C. | -99、+41 | D. | -99、41 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.02 | B. | 1.68 | C. | 1.00 | D. | 0.986 |
查看答案和解析>>
科目: 来源: 题型:选择题
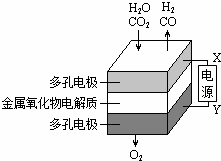 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ=H2+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2=H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该氖原子的相对原子质量为12a/b | |
| B. | Wg该氖原子的物质的量为W/aNA mol | |
| C. | Wg 该氖原子所含的质子数为 10W/a个 | |
| D. | 氖元素的摩尔质量为aNA g/mol |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
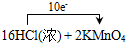 ═2KCl+2MnCl2+5Cl2↑+8H2O
═2KCl+2MnCl2+5Cl2↑+8H2O查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com