
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŅŃÖŖ¹¤ŅµÉĻŗĻ³É°±·“Ó¦N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4kJ/mol£¬»Ų“šŅŌĻĀĪŹĢā£ŗ
ŅŃÖŖ¹¤ŅµÉĻŗĻ³É°±·“Ó¦N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4kJ/mol£¬»Ų“šŅŌĻĀĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó³ĘĪŖ»ī»Æ·Ö×Ó£¬Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ/mol±ķŹ¾£®ĒėČĻÕę¹Ū²ģĻĀĶ¼£¬Č»ŗó»Ų“šĪŹĢā£ŗ
ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó³ĘĪŖ»ī»Æ·Ö×Ó£¬Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ/mol±ķŹ¾£®ĒėČĻÕę¹Ū²ģĻĀĶ¼£¬Č»ŗó»Ų“šĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆĮĖ | B£® | ĪļÖŹAµÄ×Ŗ»ÆĀŹŌö“óĮĖ | ||
| C£® | ĪļÖŹBµÄÖŹĮæ·ÖŹż¼õŠ”ĮĖ | D£® | a£¾b |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ·“Ó¦µÄ”÷S£¾0 | |
| B£® | øĆ·“Ó¦ŌŚČĪŗĪĪĀ¶ČĻĀ¾łÄÜ×Ō·¢½ųŠŠ | |
| C£® | ĻņČŻĘ÷ÖŠ³äČėÉŁĮæHe£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ | |
| D£® | ÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠĀÖʵÄĀČĖ®ŌŚ¹āÕÕĢõ¼žĻĀŃÕÉ«±äĒ³ | |
| B£® | øßŃ¹¶ŌŗĻ³É°±ÓŠĄū | |
| C£® | ½«NO2ŗĶN2O4µÄ»ģŗĻĘųĢå½µĪĀŗó£¬ĘųĢåŃÕÉ«±äĒ³ | |
| D£® | ¼ÓČė“߻ƼĮÄÜŹ¹ŗĻ³É°±µÄĖŁĀŹ¼Óæģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Čōµ„Ī»Ź±¼äÄŚÉś³ÉxmolNOµÄĶ¬Ź±ĻūŗÄx molNH3£¬Ōņ·“Ó¦“ļµ½Ę½ŗāדĢ¬ | |
| B£® | µ±»ģŗĻĘųĢåµÄŃ¹Ēæ²»ŌŁøı䣬ŌņĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ | |
| C£® | µ±»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøı䣬ŌņĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ | |
| D£® | “ļµ½»ÆŃ§Ę½ŗāŗó£¬ČōŌö“óČŻĘ÷ČŻ»ż£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
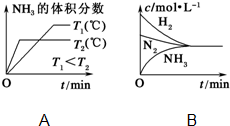
 ČēĶ¼±ķŹ¾·“Ó¦X£Øg£©?4Y£Øg£©+Z£Øg£©”÷H£¼0£¬ŌŚÄ³ĪĀ¶ČŹ±XµÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻߣ¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĆčŹöÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼±ķŹ¾·“Ó¦X£Øg£©?4Y£Øg£©+Z£Øg£©”÷H£¼0£¬ŌŚÄ³ĪĀ¶ČŹ±XµÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻߣ¬ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦µÄĆčŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | XµÄĘ½ŗā×Ŗ»ÆĀŹĪŖ85% | |
| B£® | µŚ6 min ŗ󣬷“Ó¦¾ĶÖÕÖ¹ĮĖ | |
| C£® | ČōÉżøßĪĀ¶Č£¬XµÄĘ½ŗā×Ŗ»ÆĀŹ½«“óÓŚ85% | |
| D£® | Čō½µµĶĪĀ¶Č£¬vÕż¼õŠ”£¬vÄęŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ»¶Ø“óÓŚ92.4 kJ | B£® | Ņ»¶ØŠ”ÓŚ92.4 kJ | C£® | Ņ»¶ØµČÓŚ92.4 kJ | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Zn£Øs£©+CuSO4£Øaq£©ØTZnSO4£Øaq£©+Cu£Øs£©”÷H=-216 kJ•mol-1£¬Ōņ·“Ó¦Īļ×ÜÄÜĮæ“óÓŚÉś³ÉĪļ×ÜÄÜĮæ | |
| B£® | ĻąĶ¬Ģõ¼žĻĀ£¬Čē¹ū1 molĒāŌ×ÓĖł¾ßÓŠµÄÄÜĮæĪŖE1£¬1 molĒā·Ö×ÓĖł¾ßÓŠµÄÄÜĮæĪŖE2£¬Ōņ2E1=E2 | |
| C£® | 101 kPaŹ±£¬2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-571.6 kJ•mol-1£¬ŌņH2µÄČ¼ÉÕČČĪŖ571.6 kJ•mol-1 | |
| D£® | H+£Øaq£©+OH-£Øaq£©ØTH2O£Øl£©”÷H=-57.3 kJ•mol-1£¬Ōņŗ¬1 mol NaOHµÄĒāŃõ»ÆÄĘ¹ĢĢåÓėŗ¬0.5 mol H2SO4µÄĻ”ĮņĖį»ģŗĻŗó·Å³ö57.3 kJµÄČČĮæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com