
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2O2的电子式: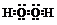 | |
| B. | 乙醇的结构式:C2H6O | |
| C. | 磷原子的结构示意图: | |
| D. | FeSO4 的电离方程式:FeSO4=Fe3++SO42ˉ |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题

 )分子中有5n个σ键
)分子中有5n个σ键| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2FeO4能与水缓慢反应生成Fe(OH)3和O2,故可用作水的消毒剂和净化剂 | |
| B. | 钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀作用 | |
| C. | 常温下氨能与氯气反应生成氯化氢和氮气,因此可用浓氨水检查氯气管道泄漏情况 | |
| D. | 开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,可能有CO32- | |
| D. | 向待测液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,待测液中一定有NH4+ |
查看答案和解析>>
科目: 来源: 题型:解答题
 氟在自然界中常以CaF2的形式存在.
氟在自然界中常以CaF2的形式存在.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cu(OH)2与盐酸,Cu(OH)2与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液,Ba(OH)2溶液与H2SO4溶液 | |
| C. | NaHCO3溶液与NaHSO4溶液,NaHCO3溶液与盐酸 | |
| D. | 石灰石与稀硝酸反应,生石灰与稀盐酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 大理石与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-=SiO${\;}_{3}^{2-}$+H2O | |
| D. | 澄清石灰水通入过量CO2的总反应:CO2+OH-=HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
 用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )
用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )| A. | 铅蓄电池放电时,该电池两极质量均减小 | |
| B. | 铅蓄电池充电时,B极应与外电源负极相连 | |
| C. | 电解苦卤水时,a电极首先放电的是Cl-而不是Br-,因为Cl-的还原性强于Br- | |
| D. | 当b极产生0.01 mol 气体时,铅蓄电池中消耗0.02 molH2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com