
科目: 来源: 题型:选择题
| A. | Fe与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 氧化铜溶于硫酸:O2-+2H+═H2O | |
| D. | NaCl溶液与AgNO3溶液反应:Ag++Cl-═AgCl↓ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 工厂利用高压电除尘,有利于减轻雾霾和预防大气污染 | |
| B. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 | |
| C. | 过滤泥水混合物,用激光笔照射滤液,能产生光亮的通路 | |
| D. | 江河入海出容易形成三角洲,如长江三角洲和黄河三角洲的形成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 50mL 1.5mol•L-1的CaCl2溶液 | B. | 100mL 3mol•L-1的NH4Cl溶液 | ||
| C. | 75mL 3mol•L-1的KCl溶液 | D. | 50mL 2mol•L-1的FeCl2溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下64g SO2含有氧原子数为1NA | |
| B. | 物质的量浓度为0.5mol•L-1的MgCl2溶液,含有Cl-数为1NA | |
| C. | 标准状况下,11.2LSO3含有的原子数目为2NA | |
| D. | 任何条件下,0.5mol N2含有分子数一定是0.5NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④⑤ | B. | ④⑤⑦ | C. | ④ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{1}{2{Q}_{2}}$ kJ | B. | Q2kJ | C. | $\frac{1}{3({Q}_{1}+{Q}_{2})}$kJ | D. | $\frac{1}{3{Q}_{1}}$kJ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  反应Ⅰ:△H>0,P2>P1 | B. |  反应Ⅱ:△H<0,T1<T2 | ||
| C. | 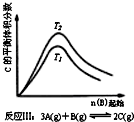 反应Ⅲ:△H<0,T2>T1;或△H>0,T2<T1 | D. | 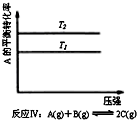 反应Ⅳ:△H<0,T2<T1或△H>0,T2>T1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 石墨转化为金刚石不是化学反应 | |
| B. | 石墨一定没有金刚石稳定 | |
| C. | 金刚石具有能量一定比石墨高 | |
| D. | 等质量的石墨与金刚石完全燃烧,石墨放出的能量多 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com