
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
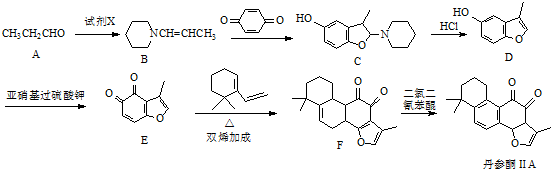
 .
. .
. 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:多选题
| 容器 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
| CO2 | H2S | H2O | |||
| Ⅰ | 607 | 0.11 | 0.41 | 0.01 | / |
| Ⅱ | 607 | 0.22 | 0.82 | / | |
| Ⅲ | 620 | 0.1 | 0.4 | / | 6.74×10-3 |
| A. | 该反应正反应为放热反应 | |
| B. | 607K时该反应的平衡常数为2.50×10-3 | |
| C. | 容器Ⅱ达到平衡时容器中COS的物质的量为0.02mol | |
| D. | 容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 制备Fe(OH)3胶体:向0.1mol•L-1FeCl3溶液中加入等体积0.3mol•L-1NaOH溶液 | |
| B. | 除去FeCl3溶液中少量Cu2+:向含有少量Cu2+的FeCl3溶液中加入适量铁粉,充分反应后过滤 | |
| C. | 比较Fe(OH)3和Al(OH)3的溶度积:向0.1mol•L-1FeCl3溶液中滴加0.1 mol•L-1氨水至不再产生沉淀,然后再滴入0.1mol•L-1AlCl3溶液,观察现象 | |
| D. | 验证氧化性Fe3+<Br2<Cl2:向试管中依次加入1mL 0.1mol•L-1FeBr2溶液、几滴KSCN溶液和1mL苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机相和水相中的现象 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | W | X | Y | Z |  |
| A | N2 | NH3 | NO | NO2 | |
| B | Na | Na2O2 | NaOH | Na2CO3 | |
| CC | Cu | CuSO4 | CuCl2 | Cu(OH)2 | |
| D | Al | Al2(SO4)3 | AlCl3 | NaAlO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 钢铁在Cl2气氛中主要发生电化腐蚀 | |
| B. | 在新制氯水中加入少量CaCO3,溶液中c(HClO)增大 | |
| C. | 反应3Cl2(g)+8NH3(g)=6NH4Cl(s)+N2(g)的△H>0,△S<0 | |
| D. | 0.1mol•L-1NaClO溶液中:c(HClO)+c(H+)=c(OH-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | MnO2与浓盐酸混合加热:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | (NH4)2Fe(SO4)2溶液中加入过量的NaOH溶液:Fe2++2OH-=Fe(OH)2↓ | |
| C. | Ba(HCO3)2溶液中加入稀硫酸:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ | |
| D. | H2C2O4(弱酸)溶液中加入酸性KMnO4溶液:2MnO${\;}_{4}^{-}$+5H2C2O4=2Mn2++10CO2↑+2H2O+6OH- |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 在化学反应中,${\;}_{1}^{1}$H2O可转变为D2O | |
| B. | “加碘食盐”生产中碘添加剂为单质I2 | |
| C. | 实验室用带玻璃塞的棕色瓶贮存液Br2 | |
| D. | 电解饱和MgCl2溶液时在阴极得到Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com