
科目: 来源: 题型:选择题
 用图所示的装置分别进行如下导电性实验,小灯泡的亮度比反应前明显减弱的是( )
用图所示的装置分别进行如下导电性实验,小灯泡的亮度比反应前明显减弱的是( )| A. | 向亚硫酸钠溶液中通入氯气 | B. | 向硝酸银溶液中通入少量氯化氢 | ||
| C. | 向氢碘酸饱和溶液中通入少量氧气 | D. | 向氢氧化钠溶液中通入少量氯气 |
查看答案和解析>>
科目: 来源: 题型:解答题
| A | B | |
| C | D |

| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10 NA | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA | |
| D. | 常温常压下,22.4L乙烯中C--H键数为4 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应中每生成1mol N2O,消耗1.5mol CO | |
| B. | B等物质的量的N2O和CO2含有相等的电子数 | |
| C. | N2O只具有氧化性,无还原性 | |
| D. | 反应中每生成1mol N2O,电子转移的物质的量为3mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4:5:2 | B. | 4:6:2 | C. | 6:4:3 | D. | 6:2:3 |
查看答案和解析>>
科目: 来源: 题型:解答题
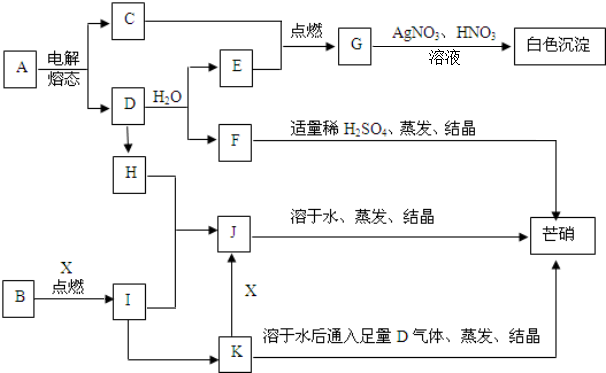
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通过澄清石灰水 | |
| B. | 先通过NaHCO3溶液,再通过澄清石灰水 | |
| C. | 通过品红溶液 | |
| D. | 先通过足量的酸性高锰酸钾溶液,再通过澄清石灰水 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

 +6NaOH$\stackrel{△}{→}$
+6NaOH$\stackrel{△}{→}$ +3NaBr+3H2O;
+3NaBr+3H2O; ;
; (写一种即可).
(写一种即可).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com