
科目: 来源: 题型:解答题
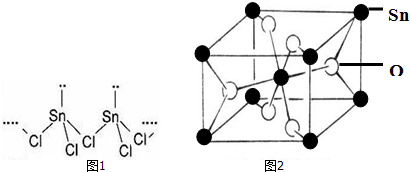
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题

 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;| 温度(℃) | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | 90℃ | 100℃ |
| NaOH | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 | 347 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 分类标准 | 氧化物 | 电解质 | |||
| 属于该类的物质 | ② | ⑧⑨ | ⑦ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向NaHSO4 溶液滴加过量的Ba(OH)2溶液H++SO${\;}_{4}^{2-}$+Ba2++OH-=BaSO4↓+H2O | |
| B. | 铁钉放入稀硫酸中2Fe+6H+=2Fe3++3H2↑ | |
| C. | 向沸水中滴入几滴饱和氯化铁溶液,并加热至溶液呈红褐色Fe3++3H2O Fe(OH)3↓+3H+ | |
| D. | 铜片与硝酸银溶液反应Cu+Ag+=Cu2++Ag |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2SO4═2H++SO${\;}_{4}^{2-}$ | B. | H3PO4?3H++PO${\;}_{4}^{3-}$ | ||
| C. | NaHCO3═Na++H++CO${\;}_{3}^{2-}$ | D. | CaCO3?Ca2++CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳的摩尔质量为12g | |
| B. | 22.4L氢气的物质的量是1mol | |
| C. | 0.1 mol•L-1的NaHSO4 溶液中,阳离子的数目之和为0.2NA | |
| D. | 1molNaCl约含6.02×1023个Cl- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com