
科目: 来源: 题型:解答题
 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:查看答案和解析>>
科目: 来源: 题型:解答题
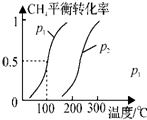 甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇:
甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{1}{4}$<$\frac{X}{Y}$<$\frac{3}{2}$ | B. | $\frac{1}{4}$<$\frac{X}{Y}$<$\frac{2}{3}$ | C. | 3<$\frac{X}{Y}$<4 | D. | 1<$\frac{X}{Y}$<3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10﹕1 | B. | 1﹕10 | C. | 2﹕9 | D. | 1﹕9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al3+ Na+NO-3 Cl- | B. | K+ Ba2+Cl- NO3- | ||
| C. | K+ Na+ Cl-AlO2- | D. | K+ Fe2+ SO42-NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
 反应:L(固)+aG(气)?bR(气)达到平衡时,温度和压强对该反应的影响如图1所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数,K表示该反应平衡常数.据此可判断( )
反应:L(固)+aG(气)?bR(气)达到平衡时,温度和压强对该反应的影响如图1所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数,K表示该反应平衡常数.据此可判断( )| A. | a>b | B. | 上述反应是吸热反应 | ||
| C. | 升温K减小 | D. | 加压K增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 达到化学平衡时,5v正(O2)=4v逆(NO) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 达到平衡前,化学反应速率关系:3v正(NH3)=2v正(H2O) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 所有酸、碱稀溶液反应的中和热相等 | |
| B. | 用铜丝替代环形玻璃搅拌棒,测得△H偏高 | |
| C. | 烧杯之间用纸屑填充的目的是避免△H偏低 | |
| D. | 实验使用的定量仪器有量筒、玻璃棒、烧杯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com