
科目: 来源: 题型:解答题
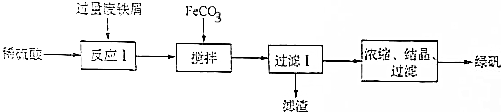

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含NA个Na+的Na2OH溶解于1L水中,Na+浓度为1mol•L-1 | |
| B. | 常温常压下,11.2LH2 中含有分分子数大于0.5NA | |
| C. | 常温常压下,30.8gCCl4中含有的原子数目为NA | |
| D. | 2L0.5mol•L-1H2O2溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目: 来源: 题型:多选题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4、O2 |
| ② | Cl2、FeCl2 | FeCl3 |
| ③ | MnO4-、Cl-、H+ | Cl2、Mn2+ |
| A. | 可以推测MnO4-、Fe2+、Na+、H+在溶液中能大量共存 | |
| B. | 第②组反应中Cl2与FeCl2的物质的量之比为2:1 | |
| C. | 第①组反应的化学方程式中KMnO4、H2O2的化学计量数之比为2:5 | |
| D. | 氧化性由强到弱的顺序为:MnO4->Fe3+>Cl- |
查看答案和解析>>
科目: 来源: 题型:填空题
 下图是盐酸与氢氧化钠溶液的滴定曲线a和b.
下图是盐酸与氢氧化钠溶液的滴定曲线a和b.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
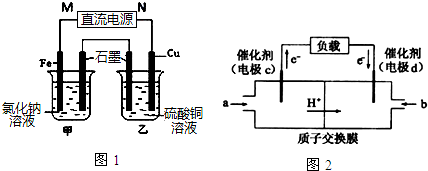
查看答案和解析>>
科目: 来源: 题型:解答题
 电化学在工业生产中有广泛应用.
电化学在工业生产中有广泛应用.查看答案和解析>>
科目: 来源: 题型:多选题
| 正 极 | 负 极 | 电解质溶液 | |
| A | Cu | Fe | FeCl3 |
| B | C | Fe | Fe(NO3)3 |
| C | Fe | Zn | Fe2(SO4)3 |
| D | Ag | Fe | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com