
科目: 来源: 题型:选择题
 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 常温时,在正负极间接上电流表或检流计,指针不偏转 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 每转移0.2mol电子,理论上生成41.4gPb | |
| D. | 正极反应式:Ca+2Cl--2e-═CaCl2 |
查看答案和解析>>
科目: 来源: 题型:选择题
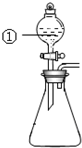 用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )| 选项 | ①中物质 | 锥形瓶中物质 | 预测锥形瓶中的现象 |
| A | 浓盐酸 | “84”消毒液 | 有黄绿色气体产生 |
| B | 浓硝酸 | 光洁的铁钉 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 先有白色沉淀生成, 后沉淀又溶解 |
| D | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色, 有黑色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
 ,氧化剂是MnO2还原剂是HCl(填化学式)
,氧化剂是MnO2还原剂是HCl(填化学式)查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 3NO2+H2O═2HNO3+NO | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 碘易溶于酒精,所以用酒精从碘水中萃取碘 | |
| C. | 液溴应保存在磨口玻璃塞试剂瓶中,并加少量水进行水封? | |
| D. | 检验某溶液是否含有SO42- 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 物质的量浓度为0.5mol/L MgCl2溶液,含有氯离子数为NA | |
| B. | 25℃、1.01×105Pa时,22gCO2中含有0.5NA个原子 | |
| C. | 46g NO2与N2O4混合气体中含有原子数为3NA | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中H+的物质的量浓度为4 mol/L |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验编号 | HCl的物质的量浓度 (mol•L-1) | BOH的物质的量浓度 (mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH>7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(OH-)>c(H+)>c(B+)>c(A-) | B. | c(B+)=c(A-) c(H+)>c(OH-) | ||
| C. | c(B+)>c(A-)>c(OH-)>c(H+) | D. | c(A-)>c(B+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com