
科目: 来源: 题型:选择题
| A. | Ca(OH)2═Ca2++2OH - | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++Cl- | D. | HNO3═H++NO3- |
查看答案和解析>>
科目: 来源: 题型:解答题
 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:查看答案和解析>>
科目: 来源: 题型:解答题
| 相关信息 | |
| X | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
 ;
;查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 | |
| C. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量小于Q kJ | |
| D. | 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
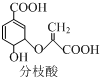
| A. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 | |
| B. | 分子中含有2种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3molNaOH发生中和反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 | |
| B. | 乙醇和水可以任意比互溶,主要是因为乙醇和水分子间能形成氢键 | |
| C. | 硫酸钡、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 | |
| D. | 煤的气化、液化和干馏均属于化学变化 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2KNO3+S+3C═K2S+N2↑+3CO2↑ | |
| B. | 2KMnO4+3H2O2+3H2SO4═2K2SO4+2MnSO4+4O2↑+6H2O | |
| C. | 5KI+KIO3+6HCl═6KCl+3I2+3H2O | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA个 | |
| B. | 500mL 1moL/L的盐酸溶液中含有的HCl分子数为0.5 NA个 | |
| C. | 将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA个 | |
| D. | 23gNa与O2反应生成Na2O和Na2O2的混合物,转移的电子数为 NA个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com