
科目: 来源: 题型:解答题
 800℃时,某密闭容器中存在如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的产率随时间的变化如图曲线I所示.
800℃时,某密闭容器中存在如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的产率随时间的变化如图曲线I所示.查看答案和解析>>
科目: 来源: 题型:解答题
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.5molO3与11.2LO2所含的分子数一定相等 | |
| B. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| C. | 常温常压下,7.0g乙烯与丁烯的混合物中含有氢原子的数目为NA | |
| D. | 标准状况下,22.4 L氯气与足量铁粉充分反应,转移的电子数为3 NA |
查看答案和解析>>
科目: 来源: 题型:解答题
 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.查看答案和解析>>
科目: 来源: 题型:解答题
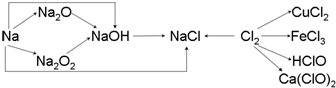
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①最多 | B. | ③最多 | C. | 一样多 | D. | 无法判断 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.6mol H2O2 | B. | 标准状况下22.4L HCl | ||
| C. | 98g H2SO4 | D. | 3.01×1023 个NH3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将金属钠保存在汽油中 | |
| B. | 将实验用剩下的钠,放回保存钠的试剂瓶中 | |
| C. | 用手掰开一块金属钠,观察钠的颜色 | |
| D. | 向盛水的烧杯中投入拇指大小的钠块,观察现象 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学家可以制造出自然界中不存在的物质 | |
| B. | 化学的特征就是认识分子和制造分子,是一门具有创造性和实用性的科学 | |
| C. | 利用化学变化可以制造出新的分子,但不能制造出新的原子 | |
| D. | 化学研究会造成严重的环境污染,最终人类将会毁灭在化学物质中 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | △H=-484kJ/mol | B. | △H=+484kJ/mol | C. | 吸收484kJ 能量 | D. | 放出484kJ能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com