
科目: 来源: 题型:选择题
 按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )| A. | 11 | B. | 12 | C. | 13 | D. | 14 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加入足量铜粉后,搅拌、可过滤可除去Cu(NO3)2溶液中混有的AgNO3 | |
| B. | 通过装有NaOH溶液的确洗气瓶来除去CO2中混有的HCl气体 | |
| C. | 某无色未知溶液中加入BaCl2溶液,有白色沉淀,可推断溶液中的一定含有SO42- | |
| D. | 未知溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则溶液中一定大量含CO32- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
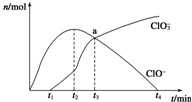 工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线:
工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  负极反应式为2H++2e-═H2↑ | B. |  阳极反应式为Ag++e-═Ag | ||
| C. |  H+向碳棒方向移动 | D. |  电解开始时阳极产生黄绿色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com