
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和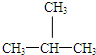
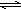 HCO3-+OH-
HCO3-+OH- 的系统命名为:3-甲基-4-乙基-庚烷
的系统命名为:3-甲基-4-乙基-庚烷 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH等于7的氨水与硫酸铵的混合溶液中c(NH4+)与c(SO42-)之比 | |
| B. | 相同温度下,1L 0.2mol/L的CH3COOH溶液与2L 0.1mol/L的CH3COOH溶液中所含的n(H+)之比 | |
| C. | NaHS溶液中c(Na+)与c(HS-)之比 | |
| D. | pH=12的KOH溶液与pH=12的Ba(OH)2溶液中c(OH-)之比 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2(蓝色石蕊试纸先变红后褪色) | B. | 氯水(pH试纸先变红后褪色) | ||
| C. | Na2S(pH试纸变红) | D. | KI(淀粉试纸变蓝) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl2+H2O?HCl+HClO | B. | FeCl3+3KSCN?Fe(SCN)3+3KCI | ||
| C. | MgCl2+2H2O?Mg(OH)2+2HCl | D. | K2CO3+H2O?KHCO3+KOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH=4.0的番茄汁中c(H+)是pH=6.0的牛奶中c(H+)的100倍 | |
| B. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 | |
| C. | AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 | |
| D. | pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com