
科目: 来源: 题型:解答题
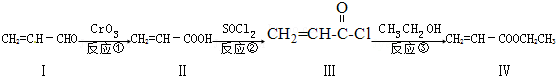
 (注明反应条件).
(注明反应条件). 或CH2=CH-O-CH2-O-CH=CH2.
或CH2=CH-O-CH2-O-CH=CH2. 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为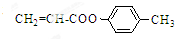 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2+H2O═H2CO3 | B. | NH4HCO3═CO2↑+H2O+NH3↑ | ||
| C. | Zn+H2SO4═H2↑+ZnSO4 | D. | Cu(OH)2+2HCl═CuCl2+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 纯盐酸 水煤气 硫酸 干冰 | |
| B. | 蒸馏水 蔗糖溶液 氧化铝 二氧化硫 | |
| C. | 胆矾 氢硫酸 铁 碳酸钙 | |
| D. | 重钙 普钙 氯化铜 碳酸钠 |
查看答案和解析>>
科目: 来源: 题型:解答题
 丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如图:
丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如图:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
查看答案和解析>>
科目: 来源: 题型:解答题


 (注明反应条件).
(注明反应条件).查看答案和解析>>
科目: 来源: 题型:解答题
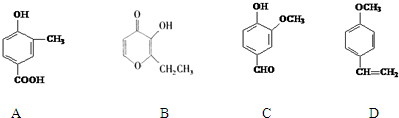
 ;
;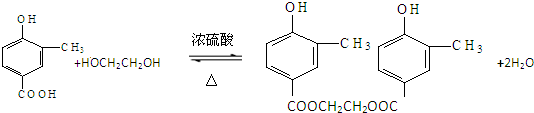 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 制取溴苯应用液溴、铁屑和苯混合,反应后先用水再用稀碱液洗涤 | |
| B. | 检验C2H5Cl中氯原子,将C2H5Cl和NaOH溶液混合加热后,加稀硫酸进行酸化 | |
| C. | 用无水乙醇和浓H2SO4共热至140℃可以制得乙烯气体 | |
| D. | 苯酚中滴加少量的稀溴水出现了三溴苯酚的白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com