
科目: 来源: 题型:选择题
| A. | 8gO2和1gH2体积为1:2 | B. | NH3和H2S密度比为1:2 | ||
| C. | 5L N2和4L CH4原子数比为1:2 | D. | 2mol CO2和1mol CO分子数比为2:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  用氯化铵和氢氧化钙制NH 3 | B. | 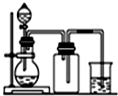 用铜片和稀硝酸制NO | ||
| C. | 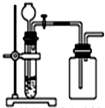 用锌粒和稀硫酸制H 2 | D. | 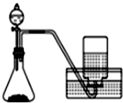 用双氧水和二氧化锰制O2 |
查看答案和解析>>
科目: 来源: 题型:解答题
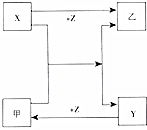 根据不同信息,回答下列问题.
根据不同信息,回答下列问题.查看答案和解析>>
科目: 来源: 题型:解答题
| 物质/25℃ | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| 溶解度/g | 1.5×10-4 | 3.0×10-3 | 9.0×10-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
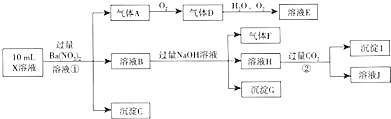
查看答案和解析>>
科目: 来源: 题型:解答题
| 物质及其杂质 | 检验 | 除杂 | |
| A | Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
| B | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
| C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3 |
| D | NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 污染物 | 来源 | |
| A | HCHO | 家具生产与使用、质量低劣的涂料的使用 |
| B | NO和NO2 | 燃煤的使用、汽车尾气 |
| C | 悬浮颗粒物 | 建筑施工、燃煤的使用 |
| D | SO2 | 雷电时在空气中产生 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氧化硅是光纤制品及现代光学的基本原料 | |
| B. | 塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 | |
| C. | 二氧化硅不与任何酸反应,可以用石英做材料制造耐酸容器 | |
| D. | 氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com