
科目: 来源: 题型:解答题
 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知: ,它的空间结构是直线型;
,它的空间结构是直线型;查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH=1的溶液中:Ca2+、Fe2+、NO3-、CO32- | |
| B. | $\frac{K}{c(OH^{-})}$=10-2mol/L的溶液中:Na+、NH4+、Cl-、NO3- | |
| C. | c(Fe3+)=0.1mol/L的溶液中:K+、SCN-、SO42-、Cl- | |
| D. | 由水电离的$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-14mol/L的溶液中:Na+、AlO2-、HCO3-、OH- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 质子数为37的氯原子:${\;}_{33}^{17}$Cl | |
| B. | Al(OH)3的电离方程式:H++AlO2═Al(0H)3═Al3++3OH- | |
| C. | CO2的结构式:O=C=O | |
| D. | 次氯酸分子的电子式: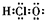 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去KNO3中混杂的NaCl | 重结晶 | 氯化钠在水中的溶解度很大 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
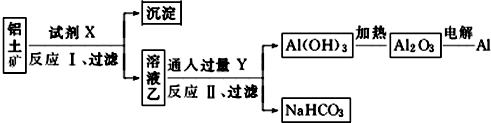
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 类别组合 | 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 |
| A | NO2 | CuO | H2SO4 | NH3•H2O | Na2S |
| B | CO2 | Na2O | CH3COOH | NaOH | NaHCO3 |
| C | SO2 | Al2O3 | HCl | KOH | NaCl |
| D | SO3 | CaO | HNO3 | Na2CO3 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
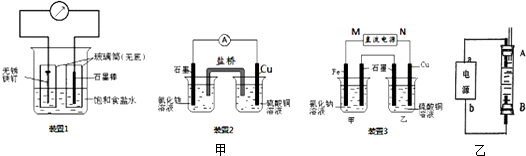
查看答案和解析>>
科目: 来源: 题型:选择题
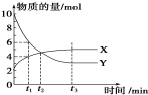 在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴、阳两极生成的气体的物质的量之比是1:1 | |
| C. | 总反应可表示为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2 | |
| D. | 阴极的反应式是:H2O+2e-═H2+O2ˉ CO2+2e-═CO+O2ˉ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA | |
| B. | 常温常压下,32g O2和O3的混合气体所含原子数为2NA | |
| C. | 标准状况下,22.4L氦气含有的分子数约为NA | |
| D. | 500mL0.2mol•L-1BaCl2溶液中Cl-浓度为0.2 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com