
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 无论n为多少,m不可能为奇数 | |
| B. | 1个C3HmOn可能含有3个醛基 | |
| C. | 当m=6、n=2时,该物质不可能含有两种官能团 | |
| D. | 当m=8时,该物质可以发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙醇与浓氢溴酸反应:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硫酸}$C6H12O6(果糖)+C6H12O6(葡萄糖) | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去 | |
| B. | 除去苯中的少量苯酚:加入NaOH溶液、振荡、静置分层后,除去水层 | |
| C. | 除去乙酸乙酯中少量的乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯 | |
| D. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  2-乙基-1,3-丁二烯 2-乙基-1,3-丁二烯 | B. |  甲苯 甲苯 | ||
| C. | CH3CH2CH2CH2OH 丁醇 | D. | HOCH2CH2CH2OH 1,3-二丙醇 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电解质溶液的pH保持不变 | |
| B. | 电流方向是由锌片流向铜片 | |
| C. | 锌片作正极,发生还原反应 | |
| D. | 锌片质量逐渐减少,铜片上有气泡产生 |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
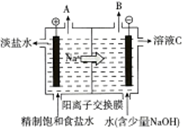 电解饱和食盐水的原理如图所示.
电解饱和食盐水的原理如图所示.查看答案和解析>>
科目: 来源: 题型:填空题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com