
科目: 来源: 题型:解答题
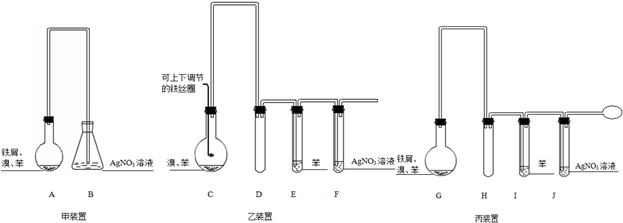
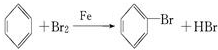 .
.| 装置的名称 | 存在的缺陷 |
查看答案和解析>>
科目: 来源: 题型:解答题
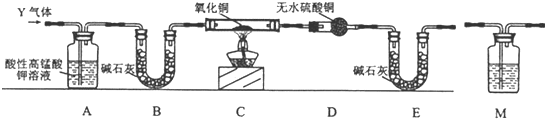
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳的燃烧热为110.5kJ/mol | |
| B. | 因为反应①中的△H<0,△S>0,所以该反应在一定条件下可以自发进行 | |
| C. | 反应①中反应物的总键能大于生成物的总键能 | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目: 来源: 题型:解答题
 硼酸(H3BO3)在食品、医药领域应用广泛.
硼酸(H3BO3)在食品、医药领域应用广泛.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
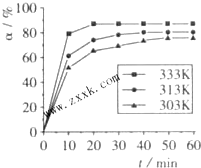
 工业上制备硫酸的过程中存在反应:2SO2(g)+O2(g)?2SO3(g) (正向放热)400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示.
工业上制备硫酸的过程中存在反应:2SO2(g)+O2(g)?2SO3(g) (正向放热)400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题

| 时间 N2的转化率 温度 | 1小时 | 2小时 | 3小时 | 4小时 |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a | b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com