
科目: 来源: 题型:选择题
| A. | NaHS溶液的水解方程式:HS-+H2O?H3O++S2- | |
| B. | 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2═4Fe3++3Br2+10Cl- | |
| C. | 向KAl(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①③⑤ | C. | ①②③④ | D. | 只有①③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使pH试纸变红的溶液:K+、Ca2+、Cl-、ClO- | |
| B. | 无色透明的溶液:Cu2+、NH4+、NO3-、CO32- | |
| C. | 0.1 mol•L-1KNO3溶液:Mg2+、Fe3+、Cl-、SO42- | |
| D. | 水电离出的c(H+)=10-12 mol•L-1的溶液:Na+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1mol/LNa2S溶液中所含S2-总数小于O.1NA | |
| B. | 若CH3COONa溶液中CH3COO-的数目为NA,则Na+的数目大于NA | |
| C. | 一定条件下,1mol N2和3 mol H2混合充分反应,转移的电子数目为6NA | |
| D. | 标准状况下,11.2 L己烷中含有的化学键数目为9.5NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用100 mL容量瓶配制50 mL 0.1 mol/L盐酸 | |
| B. | 在托盘天平上称量NaOH时,应将NaOH固体放在小烧杯中称量 | |
| C. | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL | |
| D. | 用托盘天平准确称取5.85 g NaCl固体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| B. | 自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 | |
| C. | 汽车尾气的大量排放影响了空气的质量,是造成PM2.5值升高的原因之一 | |
| D. | 明矾和氯气均可用于水的杀菌、消毒 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③④ | B. | ③④②① | C. | ④①②③ | D. | ③①②④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | KClO3中的Cl在反应中失去电子 | |
| B. | 反应中H2C2O4是还原剂 | |
| C. | ClO2是氧化产物 | |
| D. | 生成1molClO2有2 mol电子发生转移 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl2>I2>Fe3+ | B. | Cl2>Fe3+>I2 | C. | Fe3+>Cl2>I2 | D. | Fe3+>I2>Cl2 |
查看答案和解析>>
科目: 来源: 题型:解答题
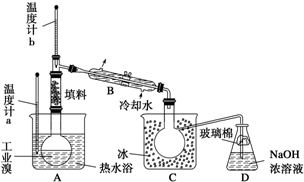 某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.他们参观生产过程后,组装了如图装置简图:
某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.他们参观生产过程后,组装了如图装置简图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com