
科目: 来源: 题型:解答题
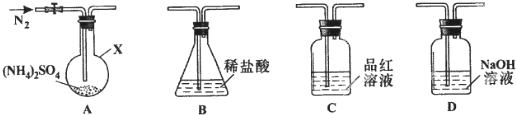
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 高中化学教材介绍了部分常见的金属与非金属元素及其化合物的相关知识,试回答下列问题
高中化学教材介绍了部分常见的金属与非金属元素及其化合物的相关知识,试回答下列问题查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤ | B. | ①④⑥ | C. | ②③⑤ | D. | ③④⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 除③外 | B. | 除④外 | C. | 除③④外 | D. | 除②⑥外 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硝酸钠固体 | B. | 冰醋酸 | C. | 硫酸锌溶液 | D. | 硫酸铜固体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀硫酸与氢氧化铜反应:H++OH-═H2O | |
| B. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 碳酸钙与盐酸反应:CO32 -+2H+═H2O+CO2↑ | |
| D. | 碳酸钾与硝酸:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
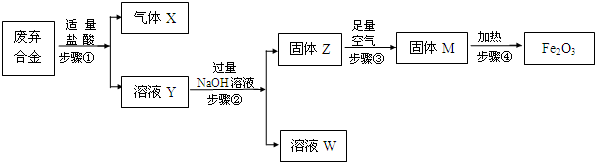
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com