
科目: 来源: 题型:解答题

| 物质 | 价格/元?吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
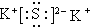 ,CO2的结构式为O=C=O.
,CO2的结构式为O=C=O.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ②③④⑤ | C. | ③⑥⑦ | D. | ②⑤⑥⑧ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②⑦ | B. | ③⑤⑧ | C. | ④⑥ | D. | ②③⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓硫酸稀释时,应该将浓硫酸沿着烧杯内壁慢慢注入装有水的烧杯中,并不断搅拌 | |
| B. | 不慎将汞滴落到桌面上,应立即用抹布抹掉,再用较多的水冲洗 | |
| C. | 甲烷易燃烧,点燃前要验纯,乙烯可以直接点燃 | |
| D. | 镁着火时可用二氧化碳扑灭 |
查看答案和解析>>
科目: 来源: 题型:选择题
 2014年世界杯足球赛在巴西举行,2016年巴西又将举办31届奥运会.奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质,能满足如图中阴影部分关系的是( )
2014年世界杯足球赛在巴西举行,2016年巴西又将举办31届奥运会.奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质,能满足如图中阴影部分关系的是( )| ① | ② | ③ | ④ | |
| A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
| B | Na2SO4 | K2SO4 | KCl | NH4Cl |
| C | NaCl | K2SO4 | KCl | NH4Cl |
| D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com