
科目: 来源: 题型:选择题
| A. | 1 L水中含有1 mol硫酸 | |
| B. | 1 L溶液中含1 mol H+ | |
| C. | 将98 g硫酸溶于1 L水所配成的溶液 | |
| D. | 从1 L溶液中取出500 mL后,剩余溶液的浓度仍为1 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NA个氧分子与NA个氢分子的质量比等于16:1 | |
| B. | 标准状况下,22.4 L以任意比混合的氢气和一氧化碳混合物所含原子数为2NA | |
| C. | 标准状况下,0.5NA个H2O分子所占体积约为11.2 L | |
| D. | 16 g O2和O3的混合物中共含有NA个氧原子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水的摩尔质量是18 g | |
| B. | 0.012 kg 12C中约含有6.02×1023个碳原子 | |
| C. | 1 mol水中约含有6.02×1023个氢原子 | |
| D. | 1 mol任何物质都含有6.02×1023个分子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③④⑤⑥⑦ | B. | ①②⑦ | C. | ①④⑤⑥ | D. | ①④⑦ |
查看答案和解析>>
科目: 来源: 题型:解答题

 .
. .
. 、
、 、
、 (任写一种)(任意写出一种结构简式).
(任写一种)(任意写出一种结构简式). )是染料工业中最重要的中间体之一,参照E的上述合成路线,设计一个以苯为原料制备苯胺的合成路线
)是染料工业中最重要的中间体之一,参照E的上述合成路线,设计一个以苯为原料制备苯胺的合成路线 .
.查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
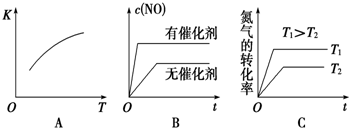
查看答案和解析>>
科目: 来源: 题型:解答题

| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 4 | 9.0 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com