
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ①④⑥ | C. | ③⑤ | D. | ①⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHCO3溶液和盐酸;CO32-+2H+═H2O+CO2↑ | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O | |
| C. | 向碳酸氢铵溶液中加过量的氢氧化钠溶液并加热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 用MnS除去MnCl2溶液中的Cu2+:MnS+Cu2+=CuS+Mn2+ |
查看答案和解析>>
科目: 来源: 题型:解答题
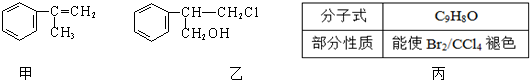
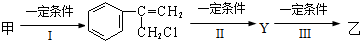
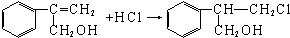 (不需注明反应条件).
(不需注明反应条件).
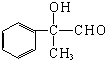 ;丙的结构简式为
;丙的结构简式为 .
. 、
、 、
、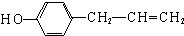 其中一种.
其中一种.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NH4HCO3溶液中加入过量NaOH溶液 HCO3-+OH-=H2O+CO32- | |
| B. | 向次氯酸钠溶液中通入少量的CO2 2ClO-+H2O+CO2=2HClO+CO32- | |
| C. | 向乙二酸(H2C2O4)溶液中滴入少量氢氧化钠溶液 H2C2O4+2OH-=C2O42-+2H2O | |
| D. | 氯化亚铁溶液中加入稀硝酸 3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com