
科目: 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:2:1 | C. | 1:1:2 | D. | 4:3:2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 相关信息 | |
| A | 所处的周期数、族序数分别与其原子序数相等 |
| B | 核外有3种不同原子轨道,每个轨道容纳的电子数相等 |
| C | 基态时,2p轨道处于半充满状态 |
| D | 与C元素处于同一周期,且D的第一电离能小于C的第一电离能 |
| E | 是目前生产、生活中应用最广泛的金属 |

 .
.查看答案和解析>>
科目: 来源: 题型:解答题

| 待测液 体积(mL) | 标准液 | |||||
| 浓度(mol/L) | 滴定前 | 滴定后 | 体积(mL) | 平均值(mL) | ||
| 第一次 | 20.00 | 0.0200 | 0.00 | 14.30 | ||
| 第二次 | 0.20 | 12.22 | ||||
| 第三次 | 0.00 | 11.98 | ||||
查看答案和解析>>
科目: 来源: 题型:多选题

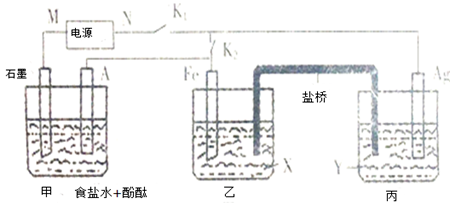
| A. | 若X是盐桥,则电子由B电极经外电路流向A电极 | |
| B. | 若X是铜条,则A电极的电极反应式是:Zn2++2e-═Zn | |
| C. | 若X是石墨条,则乙池溶液的PH不变 | |
| D. | 若X 是锌条,则A电极的质量会减小 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 图1表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点 | |
| B. | 图2表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 | |
| C. | 图3表示向Na2CO3和NaHCO3的混合溶液中滴加稀盐酸时,产生CO2的情况 | |
| D. | 图4表示向100 mL 0.1 mol/L的AlCl3和0.1 mol/L的NH4Cl混合溶液中滴加1 mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况 |
查看答案和解析>>
科目: 来源: 题型:解答题
 醋酸是日常生活中常见的弱酸.
醋酸是日常生活中常见的弱酸.
查看答案和解析>>
科目: 来源: 题型:选择题
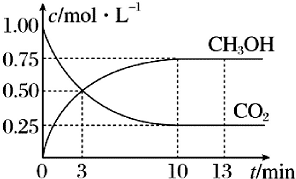 已知:CO2(g)+3H2(g)?CH5OH(g)+H2O(g)△H=-49.0kJ•mol-1一定条件下,向体积为1L的恒容密闭容器中充入1mol CO2和3mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图所示,下列叙述中正确的是( )
已知:CO2(g)+3H2(g)?CH5OH(g)+H2O(g)△H=-49.0kJ•mol-1一定条件下,向体积为1L的恒容密闭容器中充入1mol CO2和3mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化曲线如图所示,下列叙述中正确的是( )| A. | 3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 | |
| B. | 从反应开始到平衡,H2的平均反应速率v(H2)=0.225mol•L-1•min-1 | |
| C. | 13min时,向容器中充入2mol氦气,该反应的化学反应速率增大 | |
| D. | 13min时,向容器中充入2mol CO2,该反应化学平衡常数增大 |
查看答案和解析>>
科目: 来源: 题型:解答题
 已知如表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.
已知如表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.| CH2COOH | HClO | H2CO2 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com