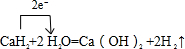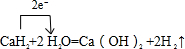A、B、C、D、E五种元素,它们的原子序数依次增大,且都是周期表中前20号元素.A原子基态时,p能级上有三个未成对电子;B元素的原子基态时,s能级与p能级的电子数相等;B、C同周期,且C是本周期中电负性最大的元素;D原子的第一至第四电离能(kJ/mol)分别为578、1817、2745、11575;E元素原子中4s能级处于全充满状态.
(1)A的氢化物沸点比同族元素其他氢化物沸点高的原因是
NH3分子间有氢键
NH3分子间有氢键
;在微电子工业中,其氢化物的水溶液可作刻蚀剂H
2O
2的清除剂,所发生反应的产物不污染环境,其化学方程式为
2NH3?H2O+3H2O2=N2↑+8H2O
2NH3?H2O+3H2O2=N2↑+8H2O
.
(2)研究表明,B、C能形成一种三原子分子,且该分子中所有原子都达到8电子稳定结构,则该分子的结构式为
F-O-F
F-O-F
.
(3)A、D两元素最高价氧化物对应的水化物能发生反应,其离子方程式为
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
.
(4)E的氢化物常做野外生氢剂,只要将其与H
2O混合立即产生大量的H
2,写出该反应的化学方程式
CaH2+2H2O=Ca(OH)2+2H2↑
CaH2+2H2O=Ca(OH)2+2H2↑
并用单线桥表示电子转移的方向和数目
.