
科目: 来源: 题型:选择题
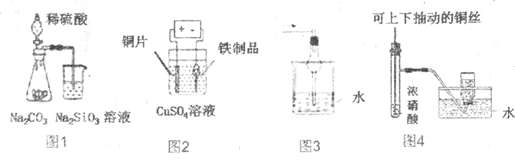
| A. | 图1为证明非金属性强弱:S>C>Si | |
| B. | 图2为在铁制品表面镀铜 | |
| C. | 图3可用于吸收氯化氢、溴化氢等气体 | |
| D. | 图4为制备并收集少量NO2气体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使酚酞变红色的溶液中:Na+、Fe3+、SO42-、Cl- | |
| B. | 饱和氯水中:K+、Na+、Cl-、HSO3- | |
| C. | 室温下,pH=13的溶液中:Na+、K+、SiO32-、Cl- | |
| D. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2SO4 Na2CO3 Ca(OH)2 | B. | HCl NaOH K2CO3 | ||
| C. | H2CO3 C2H5OH NaHSO4 | D. | Ba(OH)2 H3PO4 KOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯酸钾是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | 3mol氯气生成是有10摩尔电子转移 | |
| D. | 硫酸既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 根据是否含有氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

 B
B C
C
 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O +NaOH$\stackrel{水}{→}$
+NaOH$\stackrel{水}{→}$ .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 工业上利用Cl2和澄清石灰水反应来制取漂白粉 | |
| C. | 漂白粉的有效成分为Ca(ClO)2 | |
| D. | 除去与水反应的两个反应,图示其余转化反应均为氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com