
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
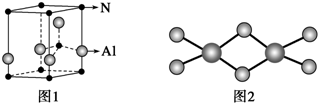
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| C. | 锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag | |
| D. | 碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-=NH3•H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ①②⑦ | D. | ①②⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(H+)/c(OH-)=1012的溶液中:NH${\;}_{4}^{+}$、Al3+、NO${\;}_{3}^{-}$、Cl- | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、F- | |
| C. | pH=7的溶液中:K+、CO32-、SO42-、Cl- | |
| D. | pH=1的溶液中:Fe2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、Na+ |
查看答案和解析>>
科目: 来源: 题型:解答题
 目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分液时,应先打开活塞放出下层液体,再关闭活塞倒出上层液体 | |
| B. | 将盛有体积比为2:1的NO和NO2混合气体的试管倒立在水中,溶液会充满试管 | |
| C. | 为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚内加热熔化 | |
| D. | 与水反应生成含氧酸的氧化物都是酸性氧化物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 三种元素的原子半径:X>Y>Z | B. | 三种元素的单质的氧化性:X>Y>Z | ||
| C. | 阴离子的还原性:X->Y2->Z3- | D. | 气态氢化物的稳定性:X<Y<Z |
查看答案和解析>>
科目: 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com