
科目: 来源: 题型:选择题
| A. | ①④ | B. | ②⑤ | C. | ③④ | D. | ①③⑤ |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5 mol1,3-丁二烯分子中含有C=C双键数为NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 取少量浑浊的天然水,加入适量明矾,天然水变得澄清透明 | |
| B. | 分别通过盛有品红溶液的洗气瓶可以鉴别SO2和CO2 | |
| C. | 保存硅酸钠溶液可以使用磨口玻璃塞、细口玻璃瓶 | |
| D. | 向Fe(OH)3胶体中逐滴加入过量的稀盐酸,先生成红褐色沉淀,最后沉淀又溶解 | |
| E. | 用镊子从煤油中夹取小块金属钠直接投入水中 |
查看答案和解析>>
科目: 来源: 题型:选择题
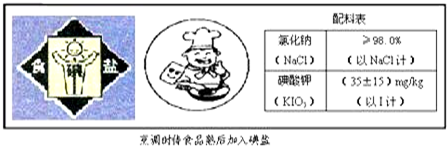
| A. | 可以用酒精从该碘盐配制的溶液中萃取KIO3 | |
| B. | “烹调时待食品熟后加入碘盐”的原因可能是碘酸钾受热易分解 | |
| C. | 1 kg此食盐中含碘酸钾(35±15)mg | |
| D. | 食用加碘盐的目的是预防龋齿 |
查看答案和解析>>
科目: 来源: 题型:解答题
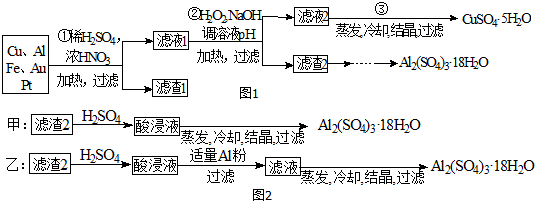
查看答案和解析>>
科目: 来源: 题型:解答题
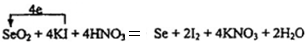 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 .
.| 离子半径 | 电负性 | 熔点 | 酸性 |
| O2-> Na+ | F>O | 金刚石> 晶体硅 | H2SO4<HClO4 |

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2═Na2O2 | |
| B. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 向NaHCO3溶液中加入足量Ba(OH)2溶液,出现白色沉淀:2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com