
科目: 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:实验题
I.某兴趣小组利用下图装置测定某硫酸工厂排放尾气中二氧化硫的含量,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。
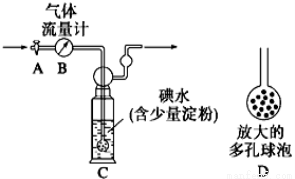
(1) C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是_____________。
(2) C中发生反应的离子方程式 。
(3) C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”、“偏低”或“无影响”)。
II.实验室常用Na2SO3固体与浓硫酸反应制取SO2 :
(4) 现有已制得SO2的饱和溶液,请利用此溶液(其他试剂任选),设计一个简单实验,比较SO2与Fe2+ 还原性的强弱(要求:写出实验步骤、现象和结论) 。
(5) 某研究小组测定部分变质的Na2SO3固体样品中Na2SO3的含量:
① 取a克Na2SO3固体样品配制成100mL溶液,取10.00mL该溶液于锥形瓶中,加入几滴淀粉溶液作指示剂,0.0100mol/L碘水进行滴定,滴定终点现象为 ,记录数据,重复滴定2次,平均消耗碘水20.00mL。
② 计算:样品中亚硫酸钠的质量分数为 。
查看答案和解析>>
科目: 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:简答题
〔化学-化学与技术〕
工业中以铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2)为原料冶炼铝过程如图所示:
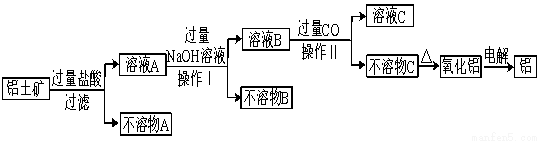
(1) 实验室进行过滤用到的玻璃仪器有烧杯、_____________、_____________。
(2) 操作II中生成不溶物C的离子方程式是 。
(3) 氧化铝的熔点高达2050℃,工业上为降低能耗,在铝的电解冶炼时,采取的措施是 。
(4) 电解冶炼铝时,阳极和阴极以碳素材料制成,电解过程中,阳极材料需定期进行更换,原因是 。
(5) 为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示:
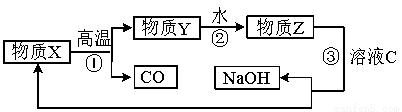
① 上述转化中未涉及四种基本反应类型中的 反应;
② 写出过程③的化学方程式: 。
(6) 研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。
查看答案和解析>>
科目: 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:填空题
【化学-物质结构与性质】氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
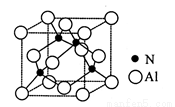
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
查看答案和解析>>
科目: 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:推断题
醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为:
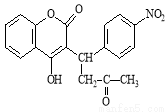
醋硝香豆素可以通过以下方法合成(部分反应条件省略)。
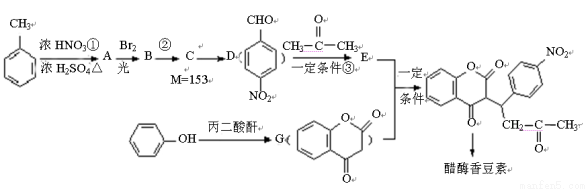
已知: + H2O
+ H2O
回答以下问题:
(1)A的结构简式为 ;反应②的反应类型 。
(2)D中含氧官能团名称是 。
(3)反应?的化学方程式为 。
(4)反应?的化学方程式为 。
(5)下列关于某些物质性质的说法正确的是 (填字母序号)。
a.醋硝香豆素的结构中含有三个苯环
b.可以用酸性高锰酸钾溶液鉴别D和E
c.E可以发生加成反应、加聚和氧化反应
d.在一定条件下,1molG最多可以和5molH2加成
(6)G的化学式为 。
(7)分子结构中只含有一个环,且同时符合下列条件的G的同分异构体共有 种。
①可与氯化铁溶液发生显色反应;
②可与碳酸氢钠溶液反应生成二氧化碳气体。
其中,苯环上的一氯代物只有两种的同分异构体的结构简式为 。
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数值,下列说法正确的是
A.1L 0.1mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
B.标准状况下,22.4L C2H4与C3H6混合气体所含有分子数为NA
C.1mol Na2O2与足量的CO2反应转移的电子数为2NA
D.18g NH 所含的电子数11NA
所含的电子数11NA
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述中不正确的是
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温 常压下,22.4L氯气与足量的镁粉充分反应,转移的电子数为2NA
常压下,22.4L氯气与足量的镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是
A.Ba2+、NO3-、NH4+、Cl- B.Ca2+、HCO3-、NH4+、AlO2-
C.K+、Ba2+、Cl-、HSO3- D.Mg2+、NH4+、SO42-、K+
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.将铁放入氯化铁溶液中:Fe+Fe3+=2Fe2+
B.向新制 的氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
的氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
C.将少量的二氧化硫通入氢氧化钠溶液中:SO2+2OH-=SO32-+H2O
D.向氯化铝溶液中加入过量的氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
A.ClO ?做还原剂 B.Fe(OH)3在反应中被还原[
?做还原剂 B.Fe(OH)3在反应中被还原[
C .高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
.高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
查看答案和解析>>
科目: 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
在酸性条件下,向含铬废水中加入FeSO4 ,可将有害的Cr2O72-转化为Cr3+,然后再加入熟石灰调节溶液的pH,使Cr3+转化为Cr(OH)3沉淀,而从废水中除 去。下列说法正确的是
去。下列说法正确的是
A.FeSO4在反应中作氧化剂
B.随着反应的进行,该废水的pH会减小
C.若该反应转移0.6 mol e-,则会有0.2 mol Cr2O72- 被还原
D.除去废水中含铬元素离子的过程包括氧化还原反应和复分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com