
科目: 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:实验题
下图是用于气体的制备.干燥.性质实验、尾气处理的常用装置。请根据要求回答下列问题。
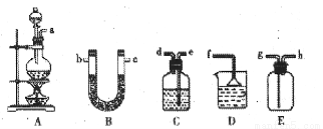
(1)怎样检查装置A的气密性 。
(2)某同学将仪器连接顺序为A-B-C-D,以此证明实验室制取Cl2的过程中有HCl和水蒸气挥发出来。
①A中反应的离子方程式是 。
②B中盛放的试剂是 ,C中盛放的是CCl4溶液,其作用是 ,D中盛放的试剂是 ,实验时看到的现象是 。
③有同学认为实验有缺陷,应该在C、D之间增加E装置,你认为该装置中.应放入 。
(3)最后,同学们用上述除B以外的仪器组装一套可以制出纯净干燥氯气的装置,按气流方向填出接口顺序a→ →ghf(不能选用B装置,其它装置可以重复使用;需要几个接口填几个).并按顺序写出所填接口对应仪器盛放的试剂 。
查看答案和解析>>
科目: 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:填空题
研究SO2、CO等大气污染气体的处理具有重要意义。
(1)利用钠碱循环法可脱除烟气中的SO2。在钠碱循环法中,用Na2SO3溶液作为吸收液吸收SO2的过程中,pH随n(SO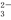 ):n(HSO
):n(HSO )变化关系如下表:
)变化关系如下表:
n(SO | 91∶9 | 1∶1 | 9∶91 |
pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显____________性,用平衡原理解释:_____________________;
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母)___________________;
a.c(Na+)=2c(SO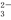 )+c(HSO
)+c(HSO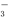 )
)
b.c(Na+)>c(HSO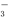 )>c(SO
)>c(SO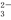 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO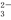 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(2)若某溶液中含3mol Na2SO3,滴入一定量的稀盐酸,恰好使溶液中Cl-和HSO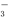 的物质的量之比为2:1,则滴入的盐酸中HCl的物质的量等于_____________mol;
的物质的量之比为2:1,则滴入的盐酸中HCl的物质的量等于_____________mol;
(3)CO可用于合成CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g) ,在一定温度压强下,在容积为2L的密闭容器中通入0.2molCO与0.4molH2,达平衡时CO的转化率50%,则该温度下的平衡常数为 ,再加入1.0molCO后重新达到平衡,则CO的转化率 (填“增大”、“不变”或“减小”),CH3OH的体积分数 (填“增大”、“不变”或“减小”);
CH3OH(g) ,在一定温度压强下,在容积为2L的密闭容器中通入0.2molCO与0.4molH2,达平衡时CO的转化率50%,则该温度下的平衡常数为 ,再加入1.0molCO后重新达到平衡,则CO的转化率 (填“增大”、“不变”或“减小”),CH3OH的体积分数 (填“增大”、“不变”或“减小”);
(4)将0.02mol/LNa2SO4溶液与某浓度BaCl2溶液等体积混合,则生成BaSO4沉淀所需原BaCl2溶液的最小浓度为 。(已知Ksp(BaSO4)=1.1×10-10)
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,实验室用如图装置模拟上述过程,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化(Co3+的还原产物是Co2+)。
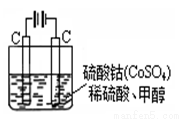
① 写出阳极电极反应式: ;
② 写出除去水中的甲醇的离子方程式: 。
查看答案和解析>>
科目: 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:填空题
氧化还原反应在生产、生话中应用广泛,用所学知识同答问题:
(1)联氨是一种可燃性液体,可用作火箭燃料。已知32.0g N2H4和H2O2反应生成氮气和水(气态),放出热量642kJ,该反应的热化学方程式是: 。
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(3)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474g KMnO4样品溶解酸化后,用0.100mol/L标准Na2S2O3溶液进行滴定,滴定至终点的现象是 。实验中,滴定至终点时消耗Na2S2O3溶液12.00mL,则该样品中KMnO4的纯度是 。(有关离子方程式为:8MnO4-+5S2O32-+14H+=8Mn2++10SO42-+7H2O)
(4)二氧化氯是目前国际上公认的最新一代的高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(5)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是____ ,又变为棕黄色的原因是 。
查看答案和解析>>
科目: 来源:2017届山西省大同市高三上学期第一次调研化学试卷(解析版) 题型:填空题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
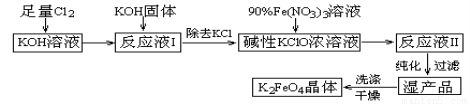
已知:
①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2 FeO4可作为新型多功能水处理剂的原因是 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为 ;
(5)在“反应液I”中加KOH固体的目的是 :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品 (写化学式)。
(7)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为 mol。
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
化学与日常生活紧密相关。下列说法中,不正确的是( )
A.甲醛可作食品防腐剂 B.氢氧化铝可作抗酸药
C.氯化钠可作食品调味剂 D.生石灰可作食品干燥剂
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.漂白粉、液氯、干冰均为混合物 B.16O和18O互为同位素
C.稀硫酸、氨水均为电解质 D.溶于水能电离出H+的物质一定是酸
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.1.0L1.0mol·L-1的NaAlO2水溶液中含有氧原子数为2NA
B.16 g O3和O2混合物中氧原子数为NA
C.25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA
D.1mol的羟基与1mol的氢氧根离子所含的电子数均为9NA
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是( )
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑
B.钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+
C.碳酸氢钠溶液与稀硫酸反应:CO32-+2H+=CO2↑+H2O
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
高铁酸钾(K2FeO4)是一种既能杀菌消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为Fe(OH)3+ClO-+OH-→FeO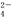 +Cl-+H2O(未配平),下列有关说法不正确的是( )
+Cl-+H2O(未配平),下列有关说法不正确的是( )
A.由上述反应可知,Fe(OH)3的氧化性强于FeO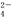
B.高铁酸钾中铁显+6价
C.上述反应中氧化剂和还原剂的物质的量之比为3∶2
D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
查看答案和解析>>
科目: 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO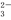 、⑥SO
、⑥SO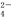 中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 | 操作 | 现象 |
(1) | 用pH试纸检验 | 溶液的pH大于7 |
(2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
(3) | 向(2)所得的水溶液中加入Ba(NO3)2溶液和稀硝酸 | 有白色沉淀产生 |
(4) | 过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀产生 |
下列结论正确的是( )
A. 不能确定的离子是① B. 不能确定的离子是③⑤
C. 肯定含有的离子是①④⑤ D. 肯定没有的离子是②⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com