
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
下列有关反应热的说法中正确的是
A.一个化学反应是否能在常温下发生与该反应的ΔH值的大小没有必然联系
B.中和热ΔH=-57.3 kJ·mol-1,所以1.00 L 1.00 mol·L-1 H2SO4与稀的NaOH溶液恰好完全反应放出57.3 kJ的热量
C.用等体积的0.50 mol·L-1盐酸、0.55 mol·L-1 NaOH溶液进行中和热测定的实验,会使测得的值偏大
D.在101 kPa时,1 mol CH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
常温下,pH=12的NaOH溶液与pH=1的HCl溶液按一定比例混合,所得溶液pH=2,则NaOH溶液与HCl溶液的体积比为
A.9∶2 B.2∶9 C.1∶9 D.10∶1
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
已知c(NH4Cl)≤0.1 mol/L时,溶液pH>5.1。现用0.1 mol/L盐酸滴定10 mL 0.05 mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为
A.10 mL B.5 mL C.大于5 mL D.小于5 mL
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:
4Al(s)+3O2(g)=2Al2O3(s) ΔH1;
4Al(s)+2O3(g)=2Al2O3(s) ΔH2;
3O2(g)=2O3(g) ΔH3。则:
A.ΔH1-ΔH2=ΔH3 B.ΔH1+ΔH2=ΔH3
C.ΔH2-ΔH1=ΔH3 D.ΔH2+ΔH1+ΔH3=0
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.1000 mol·L-1NaOH溶液滴定,下列说法正确的是
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
反应CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g) ΔH<0,达到平衡时,下列说法正确的是
CO(NH2)2(s)+H2O(g) ΔH<0,达到平衡时,下列说法正确的是
A.加入催化剂,平衡常数不变
B.减小容器体积,正、逆反应速率均减小
C.保持容积不变,增大CO2的量,NH3的转化率减小
D.降低温度,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
在一个固定容积的密闭容器中充入3 mol NO2,一定温度下建立如下平衡:2NO2 N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1 mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是
N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1 mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是
A.x>y B.x<y C.x=y D.不能确定
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:实验题
中和热的测定实验(如图)。
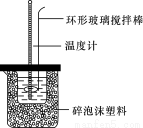
(1)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还应加入的试剂是________(填序号)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(2)在实验过程中,该同学需要测定并记录的实验数据有_____________(填序号)。
A.盐酸的浓度
B.盐酸的温度
C.氢氧化钠溶液的浓度
D.氢氧化钠溶液的温度
E.水的比热容
F.溶液混合后的最高温度
(3)若用50 mL 0.5 mol·L-1醋酸溶液代替上述盐酸测定中和热,所得数据_____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:填空题
SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:
2SO2+O2 2SO3
2SO3  ΔH<0。
ΔH<0。
请回答下列问题:
(1)判断该反应达到平衡状态的标志是_____________(填字母)。
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
(2)当该 反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是_____________(填字母)。
反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是_____________(填字母)。
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程)。
①平衡常数K=____________________;
②平衡时,SO2的转化率α(SO2)=____________________。
(4)SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3。已知NaHSO3溶液同时存在以下两种平衡:①HSO
 SO
SO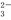 +H+,②HSO
+H+,②HSO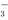 +H2O
+H2O H2SO3+OH-;常温下,0.1 mol/L NaH
H2SO3+OH-;常温下,0.1 mol/L NaH SO3溶液的pH<7,则该溶液中c(H2SO3)______________c(SO
SO3溶液的pH<7,则该溶液中c(H2SO3)______________c(SO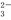 )(填“>”、“=”或“<”)。
)(填“>”、“=”或“<”)。
查看答案和解析>>
科目: 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:填空题
反应A(g)+B(s) C(g);ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“减慢”或“不变”):
C(g);ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“减慢”或“不变”):
(1)升温__________;
(2)加正催化剂__________;
(3)增大容器容积__________;
(4)加入A__________;
(5)加入C__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com