
科目: 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:填空题
在25℃时,pH = 12的NaOH溶液100 mL ,欲使它的pH降为11,需加入pH = 10的NaOH溶液___________ mL ;在25℃时,有pH为a的盐酸和pH为b的NaOH溶液等体积混合:若a+b=13,则溶液呈 性;pH为2的盐 酸和pH为12的NaOH溶液,由水电离的氢离子浓度之比为 。
酸和pH为12的NaOH溶液,由水电离的氢离子浓度之比为 。
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:填空题
25 ℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2C2O4 | H2S |
电离平衡常数 | 1.8×10-5 | Ka1=5.4×10-2 Ka2=5.4×10-5 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
请回答下列问题:
(1)H2S的一级电离常数表达式为Ka1=____________________
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序________________________
(3)H2C2O4与少量的KOH溶液反应的化学方程式:_______________________
(4)NaHS溶液与NaHC2O4溶液反应的离子方程式:_______________________
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是__________(填写序号)。
①反应所需要的时间B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量A=B
④反应过程的平均速率B>A
⑤B中有锌剩余
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:填空题
密闭容器中加入4molA、1.2molC和一定量的B三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知t0~t1阶段保持恒温、恒容,且c(B)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件,其中t3时刻为使用催化剂。

(1)若t1=15s,则t0~t1阶段的反应速率为v(C)= 。
(2)t4时刻改变的条件为 。
(3)已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q 为正值),试写出该反应的热化学方程式:__________________________
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:填空题
雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-
2SO3(g) ΔH=- 196.6 kJ·mol -1
196.6 kJ·mol -1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
(2)下图是一种用NH3脱除烟气中NO的原理。


①该脱硝原理中,NO最终转化为H2O和_____________(填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为__________L。
(3)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如右图所示,写出NO分解的化学方程式:_______________。
查看答案和解析>>
科目: 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:实验题
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充 满溶液,并使凹液面处于“0”刻度以下的位置,记下读数;
满溶液,并使凹液面处于“0”刻度以下的位置,记下读数;
②将锥形瓶用蒸馏水洗净后,直接从碱式滴定管中放入20.00mL待测溶液到锥形瓶中;
③将酸式滴定管用蒸馏水洗净后,立即向其中注入0.2000mol/L标准稀硫酸溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;
④ 向锥形瓶中滴入几滴酚酞作指示剂,进行滴定,测出所耗硫酸的体积;
向锥形瓶中滴入几滴酚酞作指示剂,进行滴定,测出所耗硫酸的体积;
⑤重复以上过程。
试回答下列问题:
(1)当滴入最后一滴稀硫酸时,____________________,可判断 达到滴定终点。
达到滴定终点。
(2)滴定过程中,下列会导致滴定结果偏低的是( )
A、若记录读数时,起始时仰视,终点时俯视
B、滴定前向锥形瓶中加入10 mL蒸馏水,其余操作正常
C、若配制硫酸时,定容时俯视刻度,其他操作正常
D、酸式滴定管在装酸液前未用待测硫酸溶液润洗
E、开始实验时碱式滴定管尖嘴部分有气泡,滴定结束气泡消失
(3)测定操作中有一步存在问题,该步骤是:__________________(填序号)
(4)根据下列数据:
滴定次数 | 待测液体积(mL) | 标准硫酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.50 | 25.45 |
第二次 | 20.00 | 4.00 | 29.05 |
第三次 | 20.00 | 3.00 | 30.00 |
第四次 | 20.00 | 2.00 | 27.00 |
请计算待测烧碱溶液的浓度为 mol/L。
(5)为了测定产品中(NH4)2Cr2O7的含量,称取样品0.150 0 g,置于锥形瓶中,加50 mL水,再加入2 g  KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10 min,加入3 mL 0.5%淀粉溶液并稀释成250ml溶液,取25ml该溶液,用0.010 0 mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00 mL,则上述产品
KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10 min,加入3 mL 0.5%淀粉溶液并稀释成250ml溶液,取25ml该溶液,用0.010 0 mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00 mL,则上述产品 中(NH4)2Cr2O7的纯度为 。(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/moL)。
中(NH4)2Cr2O7的纯度为 。(假定杂质不参加反应,已知:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-;②(NH4)2Cr2O7的摩尔质量为252g/moL)。
查看答案和解析>>
科目: 来源:2016-2017学年江西省高一上期中化学试卷(解析版) 题型:选择题
小明体检的血液检验单中,葡萄糖为5.9×10-3mol/L,表示该体检指标的物理量是( )
A.溶解度(S) B.物质的量浓度(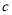 ) C.质量分数(
) C.质量分数(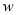 ) D.摩尔质量(M)
) D.摩尔质量(M)
查看答案和解析>>
科目: 来源:2016-2017学年江西省高一上期中化学试卷(解析版) 题型:选择题
关于粗盐提纯的下列说法正确的是 ( )
A. 溶解粗盐时,应多加水尽量使溶液稀些,防止食盐溶解不完全
B. 滤去不溶性杂质以后,将滤液移至坩埚内加热浓缩
C. 当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干
D. 将制得的晶体转移到新制过滤器中用大量水进行洗涤
查看答案和解析>>
科目: 来源:2016-2017学年江西省高一上期中化学试卷(解析版) 题型:选择题
吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”。科学家尝试用Na2SeO3消除人体内的活性氧,则在此过程中Na2SeO3的作用是( )
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.以上均不是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com