
科目: 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:填空题
按要求填写下列问题:
(1)某些共价化合物(如H2O、NH3、N2O4等)在液态时会发生微弱的电离,如:2H2O  H3O+ + OH—,则液态NH3电离的方程式是
H3O+ + OH—,则液态NH3电离的方程式是
(2)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=10,则该温度下水的KW= ,在此温度下,将pH=b的NaOH溶液Vb L与pH=a的H2SO4溶液Va L混合,若所得混合液为中性,且a+b=13,则Va:Vb=
(3)25℃时,0.1mol/L的HA溶液中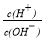 =1010.请回答下列问题:
=1010.请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”).
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是 (填字母)
A.c(HA) B.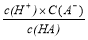 C.c(H+)与c(OH-)的乘积 D.c(OH-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
(4)在常温下,中和相同体积,相同pH的Ba(OH)2、NH3•H2O、NaOH三种稀溶液所用相同浓度的盐酸的体积分别为V1、V2、V3,则三种关系为 (用“V1、V2、V3”和“>、<、=”表示).
(5)今有A盐酸、B醋酸、C硫酸 三种酸:
①在同体积、同浓 度的三种酸中,分别加入足量的碳酸氢钠粉末,在相同条件下产生CO2的体积由大到小的顺序是 .(填写酸的序号并用符号“>、<、=”连接,下同)
度的三种酸中,分别加入足量的碳酸氢钠粉末,在相同条件下产生CO2的体积由大到小的顺序是 .(填写酸的序号并用符号“>、<、=”连接,下同)
②在同体积、同pH的三种酸中,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的氢气(同温同压下),则开始反应时速率大小关系 是 ,反应所用时间长短关系是
是 ,反应所用时间长短关系是
查看答案和解析>>
科目: 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:填空题
运用元素周期律研究元素及其化合物的性质具有重要的意义.
I.部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH和原子序数的关系如图所示.
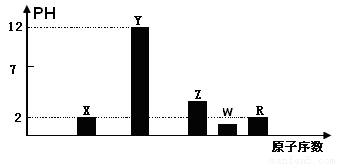
(1)元素R在周期表中的位置是
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为
(3)请写出X的最高价氧化物对应的水化物与其气态氢化物的离子反应方程式
Ⅱ.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
A.S与H2发生化合反应比C与H2化合更容易
B.酸性:H2SO3>H2CO3
C.稳定性:CH4<H2S
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似
①羰基硫(COS)的电子式为:
②羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:
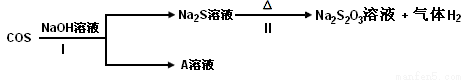
已知A是一种正盐,则反应I的化学反应方程式为
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列说法中正确的是
A. 34S原子核内中子数为16 B. 2H+的酸性比1H+的酸性更强
C. 13C和15N原子核内的质子数相差2 D. 1H216O在相同条件下比1H218O更易蒸发
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
下列说法中不正确的是
A.N2O与CO2、CCl3F与CCl2F2互为等电子体
B.CO2分子中的化学键为非极性键
C.CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化
D.NH4+为正四面体结构,可推测出PH4+也为正四面体结构
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
下列有关氢键的说法正确的是
A.氢键是一种比较弱的化学键
B.HF的稳定性很强,是因为其分子间能形成氢键
C.乙醇分子与水分子之间形成氢键,使乙醇能与水任意比互溶
D.碘化氢的沸点比氯化氢的沸点高是因为碘化氢分子之间存在氢键
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
下列叙述中正确的是
A.不同的原子之间只能构成共价化合物
B.单质中不一定存在非极性键
C.非金属原子之间只能构成共价化合物
D.有离子的物质一定有阴离子
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
苯分子不能使高锰酸钾褪色的原因是
A.分子中不存在π键 B.分子中存在6电子大π键,结构稳定
C.分子是平面结构 D.分子中只存在σ键
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
下列组合不能形成配位键的是
A.Ag+、NH3 B.H2O、H+ C.Co3+、CO D.Cu2+、H+
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
已知O3分子为V形结构,O3和O2在水中的溶解度比较正确的是
A.O3在水中的溶解度和O2一样 B.O3在水中的溶解度比O2小
C.O3在水中的溶解度比O2要大 D.没办法比较
查看答案和解析>>
科目: 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:选择题
周期表中元素的位置、原子结构与元素的性质之间关系密切。下列说法正确的是
A.锗酸(化学式为H4GeO4),是难溶于水的弱酸
B.①硫酸比次氯酸稳定;②S2-易被氯气氧化,均能说明氯元素的非金属性比硫元素强
C.中学教材所附周期表中第15列元素的最高价氧化物对应水化物的化学式均为H3RO4
D.HF的沸点比HCl 高,是因为H-F键比H-Cl键强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com