
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验Fe(NO3)2样品已被氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 |
B | 提取碘水中碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
C | 验证Mg(OH)2沉淀可以转化为 Fe(OH)3沉淀 | 向 2 mL1mol·L-1NaOH 溶液中加入2 ~3 滴 lmol·L-1MgCl2溶液,生成白色沉淀,再加入2~3滴lmol·L-1FeCl3溶液 |
D | 比较碳和硅的非金属性强弱 | 向饱和的Na2SiO3溶液中通人CO2 |
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
某有机物的结构简式如图3所示,下列有关该物质的叙述,正确的是
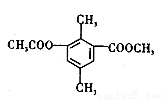
A.分子中不同化学环境的氢共有4种
B.分子中所有的碳原子不可能共平面
C.lmol该有机物与足量NaOH溶液反应,最多消耗3mol NaOH
D.能发生取代、消去、加成和氧化反应
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
下列过程都与热量变化有关,其中叙述正确的是
A.Ba(OH)2·8H2O与NH4Cl常温下混合就能反应,故该反应放热
B.已知2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol–1,故H2的燃烧热为241.8kJ·mol–1
C.已知H+-(aq)+OH-(aq)==H2O-(l)ΔH=-57.31kJ·mol–1,故Ba2+(aq)+H+(aq)+OH-(aq)+SO42-(aq)=H2O(1)+BaSO4(s)ΔH<-57.31kJ·mol–1
D.由图可知,反应C(金刚石,s)=C(石墨,s)的焓变ΔH=ΔH1-ΔH2
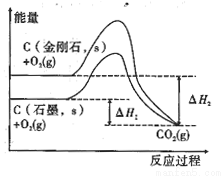
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
A、B、C、D中均含有短周期元素X, B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
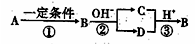
A.X元素可能是金属,也可能是非金属
B.反应①、②、③均为氧化还原反应
C.反应②、③为可逆反应
D.若B为金属单质,反应①的“一定条件”为电解时,通常加入冰晶石作为助溶剂
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
常温下,对于①0.1mol·L-1CH3COONa溶液,②pH = 13的NaOH溶液,③pH = 1的HC1溶液,④0.1mol·L-1CH3COOH溶液,[已知Ka(CH3COOH)=1.75×10-5]下列说法正确的是
A.水电离出的c(OH-):①>②>④>③
B.①和③混合后溶液呈中性:c(Na+)+c(H+)>c(CH3COO-)+c(Cl-)
C.①和④混合后溶液呈酸性: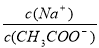 =1
=1
D.③和④分别稀释100倍后的pH:④<③
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:实验题
“一器多用”可实现多方面的化学实验探究,某课外活动小组学生利用图15所示的仪器组合(省略夹持和净化装置)来完成下列实验,回答下列问题:
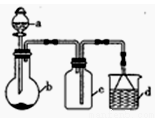
(1)仪器a的名称为______________,仪器a在使用前要________________。
(2)该装置可用于某些气体的制取、收集及尾气处理裝置,下表中3个实验的设计方案合理的是_________________(填序号)
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 稀硝酸 | Cu | NO | H2O |
B | 稀H2SO4 | CaCO3 | CO2 | NaOH溶液 |
C | 浓氨水 | NaOH固体 | NH3 | H2O |
(3)氨气和氯气接触时会产生白烟,请写出相应的化学方程式:_______________________。
(4)上述装置若a中的物质为浓硫酸,b中的物质为Cu片,在加热条件下也可制取SO2。
①下列装置可用于SO2尾气处理的是(夹持仪器已略去)_____________(填序号)。
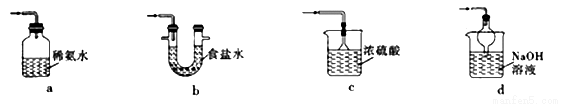
用Fe2(SO4)3溶液也可吸收多余的SO2气体.写出SO2与Fe2(SO4)3溶液反应的离子方程式:_______________________。
②某小组用反应产生的CuSO4溶液来制取胆矾,测定所得胆矾(CuSO4·xH2O)中结晶水x的值,各次 称量的数据如下表:
称量 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
质量(g) | m1=5.4 | m2=8.2 | m3=7.4 | m4=7.2 | m5=7.2 |
则胆矾应放在____________(填仪器名称)中加热;必须要进行恒重操作的原因是__________________;CuSO4·xH2O中的x=___________(保留1位小数);若测定结果x偏大,可能的原因是____________(填序号)。
a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:实验题
MnO2是一种重要的无机功能材料,MnO2的制取和在生产生活中的应用流程如图16所示:
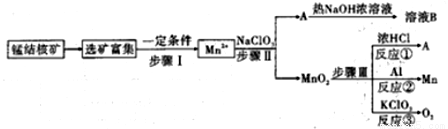
(1)步骤I中需要对富集后的矿石进行粉碎处理,其目的是__________________。
(2)步骤II中消耗0.5molMn2+时,用去1 mol·L-1的NaClO3溶液200mL,该反应离子方程式为___________________。
(3)步骤III反应②是工业冶炼金属锰的原理,化学方程式为_____________________。欲从反应③充全反应后的残渣中回收二氧化锰(难溶于水),其操作步骤是_________、烘干。
(4)已知溶液B的溶质之一(X)可循环用于步骤II中的生产,试写出A与热NaOH浓溶液反应生成X的化学方程式:_______________________。
(5)电解步骤I所得溶液也可得到MnO2,写出阳极Mn2+生成MnO2的电极反应式:__________________,阴极生成的气体产物是_____________。
(6)海底富集多种矿物结核,锰结核是其中的一种。一种质量比约为m(Mn) ∶m(Fe)=55∶448的合金 钢(其他元素略),具有抗御激烈冲击和磨损的能力,可作航母甲板等。欲通过铝热反应炼得这样的合金MnO2、Fe2O3、Al的投料比(按物质的量之比)约为 _________________。
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:填空题
SO2是评价空气质量的污染物之一,主要来源于硫酸工厂的尾气和含硫燃料的燃烧。
(1)硫酸厂尾气一般采用吸收法处理。
①已知Ka(H2SO3)=1.54x10-2,Ka(HSO3-)=1.02x10-7,Kb(NH3·H2O)=1.77x10-5,将标准状况下11.2L SO2通入到2L0.5mol·L-1的氨水中,所得溶液中溶质是__________(填化学式),该溶液呈______________(填“酸”“碱”或“中”)性。
②下列关于①所得的溶液的关系正确的是_____________(填序号)。
A.2[c(NH4+)+c(NH3·H2O)]=c(SO32-)+c(HSO3-)+c(H2SO3)
B.c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
C.c(NH4+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
D.c(NH4+)+c(OH-)=c(HSO3-)+2c(H2SO3)+c(H+)
③常温下,若用1LNaOH溶液吸收0.01mol SO2,完全吸收后溶液中c(Na+)= c(SO32-)+c(HSO3-)+ c(H2SO3),则原NaOH溶液的pH值为___________。
(2)燃煤烟气中可通过下列反应实现硫的回收:SO2(g)+2CO(g)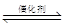 2CO2(g)+S(l)
2CO2(g)+S(l)
①该反应的平衡常数表达式是____________。
②恒温恒压下,5分钟时,反应到达平衡,气体密度减小16g·L-1,则0-5分钟内CO的反应速率是__________,若升高温度气体的密度增加,则该反应的△H__________0(填“>”或“<”)。
③下列措施,既能提高该反应的反应速率,又能提高SO2的吸收率的是__________(填序号)。
A. 加压 B.增加SO2的浓度
B. 升高温度 D.移走产物
(3)SO2还能被多种物质吸收。
①写出SO2与Ba(NO3)2溶液反应的离子方程式:_______________。
②如果用含等物质的量溶质的下列个溶液分别吸收SO2,则理论吸收量由多到少的顺序是__________(用序号排序)。
A. H2S B.Na2SO3
C.BaCl2 D.酸性KMnO4
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
储氢合金是利用金属或合金与氢形成氢化物而把氢储存起来。MgH2,LaNi5,MmNiMn(Mm代表混合稀土)等是几类常见的储氢材料。近期,中国科大的最新研究发现,在镍的表面覆盖石墨烯(如图所示),可以大大增加储氢材料释放氢气的速率。已知:石墨烯是一种由单层碳原子组成的平面结构,具有良好的导电、导热性。回答下列问题:
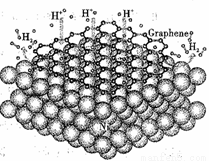
(1)Mn的价电子排布式为_______________,据此可判断Mn元素在元素周期表中处于_________区。
(2)①石墨烯中碳原子的杂化方式为_______________,据此说明石墨烯具有良好导电性的原因是_____________________。
②Si是与C相邻的同主族元素,据原子结构分析并预测,Si能否形成类似石墨烯的稳定结构?
________________________。
(3)碳与氢能形成乙烷、乙烯、乙炔等多种有机物。巳知,在相同条件下,乙烯,乙炔易与氢气加成, 最终生成乙烷。
①乙烷的二溴代物中____________(填“有”或“无”)手性分子。
②从共价键的形成过程说明乙烯比乙烷活泼的原因:____________________。
③C—C,C C,C
C,C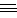 C的键能之比最有可能为___________(填序号)。
C的键能之比最有可能为___________(填序号)。
A.1.00∶2.17:4.90
B.1.00∶1.77∶2.34
C.1.00:2.00∶3.00
(4)Ni晶体中微粒之间的作用力为________。Ni的晶胞棋型与铜、银、金相同,用Ni的微粒半径(rNi)列出Ni晶体的空间占有率的表达式:__________________。
查看答案和解析>>
科目: 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:推断题
【化学——选修5:有机化学基础】功能高分子P的合成路线如图24所示:
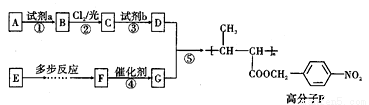
已知:①A为芳香烃,其核磁共振氢谱显示有4组峰,其峰面积之比为3∶2∶2∶1;
②E的产量可用来衡量一个国家石油化工发展的水平。
(1)A的结构简式为__________________,试剂a是__________________。
(2)反应③的化学方程式是__________________________。
(3)F的分子式是C4H6O2,F中含有的官能团名称是___________________。
(4)反应④的类型_______________________。
(5)反应⑤的化学方程式是_____________________________。
(6)已知:2CH3CHO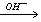
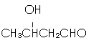 ,以E为起始原料.选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,以E为起始原料.选用必要的无机试剂合成F,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com