
科目: 来源:2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷(解析版) 题型:选择题
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是
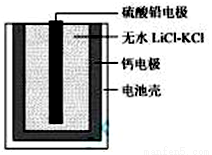
A.正极反应式:Ca + 2Cl--2e- = CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1mol电子,理论上生成10.35 g Pb
查看答案和解析>>
科目: 来源:2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷(解析版) 题型:填空题
回答下列问题:
(1)某工业废水中含有一定量的Cr2O72-和CrO42-,二者存在平衡:
2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
①若平衡体系滴加少量H2SO4(不考虑温度的影响),溶液显________色.。
②能说明该反应达平衡状态的是_____________。
a.Cr2O72-和CrO42-的浓度相同
b.2v (Cr2O72-)=v (CrO42-)
c.溶液的颜色不变
(2)H2O2稀溶液易被催化分解,可使用的催化剂为(填序号)____________。
a.MnO2 b.FeCl3
c.Na2SO3 d.KMnO4.
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为N2(g)+O2(g) 2NO(g)ΔH>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是:___________________。
2NO(g)ΔH>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是:___________________。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:____ _____________。
③目前,火箭残骸中常出现红棕色气体,原因为:N2O4(g) 2NO2(g)当温度升高时,气体颜色变深,则反应为______(填“吸热”或“放热”)反应。
2NO2(g)当温度升高时,气体颜色变深,则反应为______(填“吸热”或“放热”)反应。
查看答案和解析>>
科目: 来源:2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷(解析版) 题型:填空题
(1)H2S是一种无色、有臭鸡蛋气味的气体、有剧毒。是一种大气污染物。它的燃烧热△H=-a kJ/mol, 写出H2S燃烧热的热化学方程式为:____________。
(2)己知:Mg(s)+ 2 H2O (g)= Mg(OH )2(s)+H2(g)△H1=441- kJ/mol、H2O(g)=1/2H2(g)+O2(g)△H2=242kJ•mol-1、Mg(s)+1/2O2(g)=MgO(s)△H3=-602kJ•mol-1。
①Mg(OH )2分解的热化学方程式为:__________________。
②Mg(OH )2可以作为阻燃剂的原因(写一条即可)_____________。
(3)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。针对此现象,某同学认为该反应放热,温度升高,反应速率加快。
①从影响反应速率的因素看,你的猜想还可能是_____________的影响
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,可以在反应一开始时加入
A、硫酸钾 B、硫酸锰 C、氯化锰 D、水
(4)已知化学反应:①Fe(s)+CO2(g) FeO(s)+CO(g);②:Fe(s)+H2O(g)
FeO(s)+CO(g);②:Fe(s)+H2O(g) FeO(s)+H2(g);③:CO2(g)+H2(g)
FeO(s)+H2(g);③:CO2(g)+H2(g) CO(g)+H2O(g)。三个反应的平衡常数分别为K1、K2和K3。推断反应③为△H3____0(填“ > ”成“ < ”),根据反应①和反应②可推导出K1、K2和K3的关系式:_______________。
CO(g)+H2O(g)。三个反应的平衡常数分别为K1、K2和K3。推断反应③为△H3____0(填“ > ”成“ < ”),根据反应①和反应②可推导出K1、K2和K3的关系式:_______________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b.的代数式表示该混合溶液中醋酸的电离常数为:____________。
查看答案和解析>>
科目: 来源:2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷(解析版) 题型:实验题
完成下列问题:
I.(1)某学习小组用0.80 mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸。
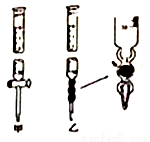
①滴定管如图所示,用 (填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸溶液。
②用滴定的方法来测定盐酸的浓度,实验数据如下所示:
实验编号 | 待测盐酸溶液的体积/mL | 滴入NaOH溶液的体积/mL |
1 | 20.00 | 23.00 |
2 | 20.00 | 23.10 |
3 | 20.00 | 22.90 |
该未知盐酸的浓度为_______________(保留两位有效数字)。
(2)若用酚酞作指示剂,达到滴定终点的标志是____________________。
(3)造成测定结果偏高的操作可能是__________。
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的读数时,滴定前仰视凹液面最低处,滴定后俯视读数
II.为了测定某氯化锶(SrCl2)样品的纯度,探究活动小组设计了如下方案:
①称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。
②用含Fe3+的溶液作指示剂,用0.2 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。
请回答下列问题:
(1)用含Fe3+的溶液作指示剂达到滴定终点时发生颜色变化的离子方程式:_____________。
(2)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源:2016-2017学年天津市武清区等五区县高三上学期期中考试化学试卷(解析版) 题型:实验题
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
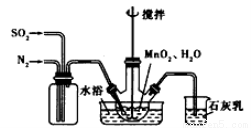
(1)制备MnSO4溶液:在烧瓶中(装置见上图)加入一定量MnO2和水,搅拌,通人SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤。
①写出反应方程式:MnO2+ H2SO3=_________________;
石灰乳参与反应的化学方程式为___________________。
②反应过程中,为使SO2尽可能转化完全,在通人SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有(填两种)________________、___________________。
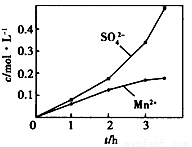
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如上图。导致溶液中Mn2+、SO42-的浓度变化产生明显差异,其中Mn2+对O2与H2SO3反应所起的作用是_________________。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH= 7.7。
请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2O 、Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①边搅拌边加入_________________,并控制溶液pH_______7.7;
②_______________________;
③_______________________;
④_______________________;
⑤低于100℃干燥。
查看答案和解析>>
科目: 来源:2017届福建省泉州市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
“绿色生活,可持续发展”是上海世博会的主题。下列有关环境、健康可持续发展的叙述中,正确的是( )
①在饲料中加入“瘦肉精”,人食用猪肉后能降低“高血脂”的发病率;
②自备购物袋,不用塑料袋;
③建立空调液化水和屋面雨水收集系统,充分利用水资源;
④大力发展、推广可利用太阳能、风能的城市照明系统;
⑤可吸入颗粒(例如硅酸盐粉尘)形成气溶胶,对人类健康危害较大;
⑥用填埋法处理未经分类的生活垃圾。
A.②③④⑤ B.②③④⑥ C.①②③④ D.③④⑤⑥
查看答案和解析>>
科目: 来源:2017届福建省泉州市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
下列反应的离子方程式表示正确的是( )
A.浓盐酸与铁屑反应:2Fe+6H+===2Fe3++3H2↑
B.Al与CuSO4溶液反应:Al+Cu2+===Cu+Al3+
C.NaHSO3溶液与氢碘酸反应:HSO3- +HI===H2O+SO2↑+I-
D.向FeCl3溶液中加入石灰乳:3Ca(OH)2+2Fe3+===2Fe(OH)3+3Ca2+
查看答案和解析>>
科目: 来源:2017届福建省泉州市高三上学期第一次阶段考化学试卷(解析版) 题型:选择题
某离子反应涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中c(NH4+)随着反应的进行逐渐减小。下列判断正确的是( )
A.还原产物是N2
B.消耗1 mol氧化剂,转移电子3 mol
C.氧化剂与还原剂的物质的量之比为2∶3
D.反应后溶液的酸性明显增强
查看答案和解析>>
科目: 来源:2016-2017学年江苏省沭阳县高一上学期期中化学试卷(解析版) 题型:选择题
实验室里有4个药品橱,已经存放以下列试剂:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 醋酸,乙醇 | CuSO4·5H2O,MgCl2 | 白磷,硫黄 | 镁条,锌粒 |
实验室新购 进一些碘化钾,应该将这些碘化钾放在
进一些碘化钾,应该将这些碘化钾放在
A.甲橱 B.乙橱 C.丙橱 D.丁橱
查看答案和解析>>
科目: 来源:2016-2017学年江苏省沭阳县高一上学期期中化学试卷(解析版) 题型:选择题
以下化学用语及对应表达正确的是
A.H218O 的摩尔质量为20g?mol-1
B.铁粉溶于盐酸的化学方程式:2Fe + 6HCl = 2FeCl3 + 3H2↑
C.氯离子的结构示意图: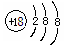
D.乙醇的分子式为CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com