
æĘÄæ£ŗ Ą“Ō“£ŗ2016-2017ѧğŗŚĮś½Ź”øßŅ»ÉĻŌĀæ¼Čż»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
½«×ÜĪļÖŹµÄĮæĪŖn molµÄÄĘŗĶĀĮ£ØĘäÖŠÄʵÄĪļÖŹµÄĮæ·ÖŹżĪŖx£©£¬Ķ¶ČėŅ»¶ØĮæµÄĖ®ÖŠ³ä·Ö·“Ó¦£¬¹²ŹÕ¼Æµ½±ź×¼×“æöĻĀµÄĘųĢåV L£®°“ŅŖĒóĢīæÕ£ŗ
£Ø1£©x=0.5Ź±£¬V= £ØÓĆŗ¬nµÄ“śŹżŹ½±ķŹ¾£©”£
£Ø2£©Čō½šŹōÓŠŹ£Óą£¬ŌņxµÄȔֵ·¶Ī§ĪŖ£ŗ
£Ø3£©Čō½šŹōƻӊŹ£Óą£¬ŌņVµÄȔֵ·¶Ī§ĪŖ£ŗ £ØÓĆŗ¬nµÄ“śŹżŹ½±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓėČÕ³£Éś»ī”¢Éś²śµČĆÜĒŠĻą¹Ų”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A£®Ź¹ÓĆLEDÕÕĆ÷µĘŹōÓŚ”°µĶĢ¼Éś»ī”±·½Ź½
B£®ŃŠÖĘøߊŌÄܵÄÄĶÄ„ĀÖĢ„£¬æɼõÉŁĻøæÅĮ£Īļ£ØPM2£®5£©µÄ²śÉś
C£®ŌŚ¼ŅÓƵēČČĖ®Ę÷²»ŠāøÖÄŚµØĻāĒ¶Ć¾°ō£¬ŅŌ·ĄÖ¹ÄŚµØ±»øÆŹ“
D£®Ź©ÓĆŹŹĮæŹÆ»ŅČéæɽµµĶŃĪ¼īµŲ£Øŗ¬½Ļ¶ąNaCl”¢Na2CO3£©µÄ¼īŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżÖµ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A£®±ź×¼×“æöĻĀ£¬22£®4 LŅŅĶéÖŠĖłŗ¬¹²¼Ū¼üŹżÄæĪŖ6NA
B£®100 mL0£®1 mol£®L-1 FeCl3ČÜŅŗÖŠŗ¬ÓŠFe3+µÄŹżÄæĪŖ0£®01NA
C£®0£®2 mol ZnÓėŅ»¶ØĮæÅØĮņĖįĒ”ŗĆĶźČ«·“Ó¦£¬Éś³ÉµÄĘųĢå·Ö×ÓŹżĪŖ0£®2NA
D£®1 L0£®1 mol£®L-l NaHCO3ČÜŅŗÖŠHC03-ŗĶCO32-Ąė×ÓŹżÖ®ŗĶĪŖ0£®1NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ŲÓŚÓŠ»śĪļµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ÄĘøśŅŅ“¼·“Ó¦±ČøśĖ®·“Ó¦¾ēĮŅ
B£®ÓŠ»śĪļClCH2COOHÖŠŗ¬ÓŠĮ½ÖÖ¹ŁÄÜĶÅ
C£®½«±½ÓėÅØĻõĖį”¢ÅØĮņĖį¹²ČČŅŌÖĘČ”±½»ĒĖį
D£®½«ŅŅĶéŗĶĀČĘų»ģŗĻŗó¹āÕÕÖʱø“æ¾»µÄĀČŅŅĶé
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠøł¾ŻŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ£Ø £©
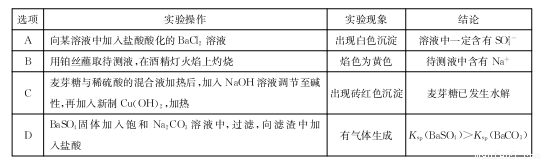
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ŖŹ¢¶Ł“óѧµÄŃŠ¾æĶŶӲÉÓĆŠĀŠĶµÄĢ«ŃōÄÜČČ¹ż³ĢÉś²śĖ®Äą£¬æÉŹµĻÖC02ĮćÅÅ·Å”£µ±µē½āµĶÓŚ800”ę Ź±£¬Ģ¼ĖįøĘĻČ·Ö½ā³ÉĪŖCaOŗĶCO2£¬µē½āÖŹĪŖČŪČŚµÄĢ¼ĖįÄĘ£¬»ł±¾ŌĄķČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
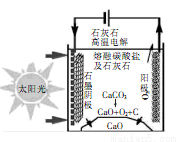
A£®Éś²ś¹ż³ĢÖŠÄÜĮæ×Ŗ»Æ·½Ź½ŹĒ¹āÄÜ”¢µēÄÜ×Ŗ»ÆĪŖ»ÆѧÄÜ
B£®ŹÆÄ«µē¼«µÄµē¼«·“Ó¦Ź½ĪŖ3CO2 +4e- =C+ 2CO32-
C£®µē½ā¹ż³ĢÖŠČŪČŚĢ¼ĖįÄʵÄĪļÖŹµÄĮæ²»·¢Éś±ä»Æ
D£®µē½ā¹ż³ĢÖŠČō²śÉś11£®2 LO2£¬Ōņ×ŖŅĘ2 molµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®³£ĪĀĻĀ£¬pH=2µÄŃĪĖįÓėĮņĖįµÄ»ģŗĻČÜŅŗÖŠ£ŗ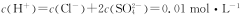
B£®Ä³0£®1 mol£®L-lµÄNaHAČÜŅŗµÄpH=4£¬øĆČÜŅŗÖŠ£ŗ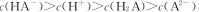
C£®NaOHÓėCH3 COOH»ģŗĻĖłµĆČÜŅŗÖŠĄė×ÓÅØ¶Č²»æÉÄÜŹĒ£ŗ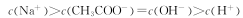
D£®µČÅØ¶ČµÄNa2 C03ČÜŅŗÓėNaHC03ČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ£ŗ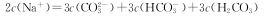
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ”£m”¢n”¢pŹĒÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ¶žŌŖ»ÆŗĻĪļ£¬rŹĒŌŖĖŲYµÄ³£¼ūµ„ÖŹ£¬ÄÜŹ¹“ų»šŠĒµÄľĢõø“Č¼£¬qµÄĖ®ČÜŅŗ³Ź¼īŠŌ£¬0£®0l mol£®L-l sČÜŅŗµÄpHĪŖ12£¬q”¢sµÄŃęÉ«·“Ó¦¾ł³Ź»ĘÉ«”£ÉĻŹöĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
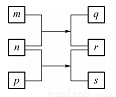
A£®Ō×Ó°ė¾¶£ŗW<X<Y<Z
B£®Ķس£×“æöĻĀ£¬XµÄĒā»ÆĪļæÉÄܳŹĘųĢ¬”¢ŅŗĢ¬»ņ¹ĢĢ¬
C£®YµÄĒā»ÆĪļµÄ·Šµć±ČZµÄĒā»ÆĪļµÄ·Šµćøß
D£®ÓÉW”¢X”¢Y”¢ZĖÄÖÖŌŖĖŲÖ»ÄÜ×é³ÉŅ»ÖÖ»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
Ēč»ÆÄĘ£Ø»ÆѧŹ½NaCN£¬CŌŖĖŲ+2¼Ū£¬NŌŖĖŲ-3¼Ū£©ŹĒ°×É«½į¾§æÅĮ£”¢Ņ׳±½ā”¢¾ē¶¾”¢Ņ×ČÜÓŚĖ®”¢Ė®ČÜŅŗ³Ź¼īŠŌ”£Ēč»ÆÄĘŠ¹Ā©£¬æÉŅŌĶعżÅēČ÷Ė«ŃõĖ®»ņĮņ“śĮņĖįÄĘČÜŅŗĄ““¦Ąķ£¬ŅŌ¼õĒįĪŪČ¾”£
£Ø1£©Ēč»ÆÄĘČÜŅŗ³Ź¼īŠŌ£¬ĘäŌŅņŹĒ £ØÓĆĄė×Ó·½³ĢŹ½½āŹĶ£©”£
£Ø2£©ÓĆĖ«ŃõĖ®“¦ĄķNaCN²śÉśŅ»ÖÖĖįŹ½ŃĪŗĶŅ»ÖÖÄÜŹ¹ŹŖČóŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ壬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________”£
ij»ÆѧŠĖȤŠ”×éŌŚŹµŃéŹŅÖʱøĮņ“śĮņĖįÄĘ£¬²¢¼ģ²āŗ¬Ēč»ÆÄĘ·ĻĖ®ÓĆĮņ“śĮņĖįÄĘČÜŅŗ“¦ĄķŗóÄÜ·ń“ļ±źÅÅ·Å”£
”¾ŹµŃéŅ»”æŹµŃéŹŅĶعżČēĻĀĶ¼ĖłŹ¾×°ÖĆÖʱøNa2S2O3”£
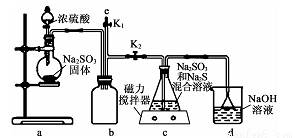
£Ø3£©×°ÖĆaÖŠŹ¢×°Na2 S03¹ĢĢåµÄŅĒĘ÷Ćū³ĘŹĒ £¬×°ÖĆbµÄ×÷ÓĆŹĒ________”£
£Ø4£©×°ÖĆcÖŠµÄ²śĪļÓŠNa2S2O3ŗĶCO2ĘųĢåµČ£¬ŹµŃé½įŹųŗó£¬×°ÖĆdÖŠµÄČÜÖŹÓŠNaOH”¢Na2CO3£¬»¹æÉÄÜÓŠ £ØĢī»ÆѧŹ½£©”£
£Ø5£©ŹµŃé½įŹųŗó£¬ŌŚe“¦×īŗĆĮ¬½ÓŹ¢____£ØĢī”°NaOHČÜŅŗ”±”°Ė®”±»ņ”°CCl4”±£©µÄ×¢ÉäĘ÷£¬ŌŁ¹Ų±ÕK2“ņæŖK1£¬·ĄÖ¹²š³ż×°ÖĆŹ±ĪŪČ¾æÕĘų”£
”¾ŹµŃ鶞”æ²ā¶ØÓĆĮņ“śĮņĖįÄĘČÜŅŗ“¦ĄķŗóµÄ·ĻĖ®ÖŠĒč»ÆÄʵÄŗ¬Į攣ŅŃÖŖ£ŗ
¢Ł·ĻĖ®ÖŠĒč»ÆÄʵÄ×īøßÅŷűź×¼ĪŖ0£®50 mg£®L-l”£
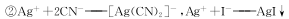 £¬AgI³Ź»ĘÉ«£¬ĒŅCN-ÓÅĻČÓėAg+·“Ó¦£¬
£¬AgI³Ź»ĘÉ«£¬ĒŅCN-ÓÅĻČÓėAg+·“Ó¦£¬
ŹµŃéČēĻĀ£ŗČ”25£®00 mL“¦ĄķŗóµÄĒč»ÆÄĘ·ĻĖ®ÓŚ×¶ŠĪĘæÖŠ²¢µĪ¼Ó¼øµĪKIČÜŅŗ×÷ÖøŹ¾¼Į£¬ÓĆ1£®000”Į1 0-4mol£®L-lµÄ±ź×¼AgNO3ČÜŅŗµĪ¶Ø£¬ĻūŗÄAgNO3ČÜŅŗµÄĢå»żĪŖ2£®50 mL”£
£Ø6£©µĪ¶ØÖÕµćµÄÅŠ¶Ļ·½·ØŹĒ________”£
£Ø7£©“¦ĄķŗóµÄ·ĻĖ®ÖŠĒč»ÆÄʵÄŗ¬ĮæĪŖ mg£®L-l”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”Ō„±±ĶĘ¼öøßČżÉĻѧʌ¾«Ó¢¶Ōæ¹Čü»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
µŖŃõ»ÆĪļŹĒÄæĒ°Ōģ³É“óĘųĪŪČ¾µÄÖ÷ŅŖĘųĢ唣NOŌŚæÕĘųÖŠ“ęŌŚČēĻĀ·“Ó¦£ŗ

£Ø1£©ÉĻŹö·“Ó¦·ÖĮ½²½Ķź³É£¬ĘäÖŠµŚŅ»²½·“Ó¦¢ŁČēĻĀ£¬Š“³öµŚ¶ž²½·“Ó¦¢ŚµÄČČ»Æѧ·½³ĢŹ½£ØĘä·“Ó¦µÄģŹ±ä
”÷H2ÓĆŗ¬”÷H”¢”÷H1µÄŹ½×ÓĄ“±ķŹ¾£©£ŗ
¢Ł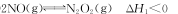
¢Ś________”£
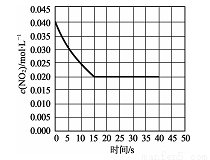
£Ø2£©ŌŚÄ³ĪĀ¶ČĻĀµÄŅ»ĆܱÕČŻĘ÷ÖŠ³äČĖŅ»¶ØĮæµÄN02·¢ÉśÉĻŹö·“Ó¦£¬²āµĆNO2µÄÅضČĖꏱ¼äµÄ±ä»ÆĒśĻßČēĻĀĶ¼ĖłŹ¾£¬Ē°5ĆėÄŚO2µÄĘ½¾łÉś³ÉĖŁĀŹĪŖ mol£®L-1£®s-l£¬øĆĢõ¼žĻĀ·“Ó¦£ŗ2NO+O2 2NO2µÄ»ÆŃ§Ę½ŗā³£ŹżŹżÖµĪŖ £¬Ę½ŗāŗóijŹ±æĢ£¬Éżøß·“Ó¦ĢåĻµµÄĪĀ¶Č£¬½ØĮ¢ŠĀĘ½ŗāדĢ¬ŗ󣬲āµÄ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæŠ”ÓŚŌĘ½ŗāדĢ¬£¬Ōņ£ŗ2NO£Øg£©+O2 £Øg£©
2NO2µÄ»ÆŃ§Ę½ŗā³£ŹżŹżÖµĪŖ £¬Ę½ŗāŗóijŹ±æĢ£¬Éżøß·“Ó¦ĢåĻµµÄĪĀ¶Č£¬½ØĮ¢ŠĀĘ½ŗāדĢ¬ŗ󣬲āµÄ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæŠ”ÓŚŌĘ½ŗāדĢ¬£¬Ōņ£ŗ2NO£Øg£©+O2 £Øg£© 2NO2 £Øg£©”÷H £ØĢī”°>”±»ņ”°<”±£©0”£
2NO2 £Øg£©”÷H £ØĢī”°>”±»ņ”°<”±£©0”£
£Ø3£©2NO£Øg£©+O2£Øg£© 2NO2 £Øg£©µÄĮ½²½·“Ó¦ÖŠ£¬·“Ó¦¢ŁµÄ·“Ó¦ĖŁĀŹŹżÖµ½Ļ“ó£¬ŹĒŅ»øöæģ·“Ó¦£¬»įæģĖŁ½ØĮ¢Ę½ŗāדĢ¬£¬¶ų·“Ó¦¢ŚŹĒŅ»øöĀż·“Ó¦£¬Ōņ¾ö¶Ø·“Ó¦2NO£Øg£©+O2 £Øg£©
2NO2 £Øg£©µÄĮ½²½·“Ó¦ÖŠ£¬·“Ó¦¢ŁµÄ·“Ó¦ĖŁĀŹŹżÖµ½Ļ“ó£¬ŹĒŅ»øöæģ·“Ó¦£¬»įæģĖŁ½ØĮ¢Ę½ŗāדĢ¬£¬¶ų·“Ó¦¢ŚŹĒŅ»øöĀż·“Ó¦£¬Ōņ¾ö¶Ø·“Ó¦2NO£Øg£©+O2 £Øg£© 2NO2 £Øg£©·“Ó¦ĖŁĀŹµÄŹĒ·“Ó¦________£ØĢī”°¢Ł”±»ņ”°¢Ś”±£©£»¶Ō£Ø2£©ÖŠ·“Ó¦ĢåĻµÉżøßĪĀ¶ČµÄ¹ż³ĢÖŠ£¬·¢ĻÖ2NO£Øg£©+O2 £Øg£©
2NO2 £Øg£©·“Ó¦ĖŁĀŹµÄŹĒ·“Ó¦________£ØĢī”°¢Ł”±»ņ”°¢Ś”±£©£»¶Ō£Ø2£©ÖŠ·“Ó¦ĢåĻµÉżøßĪĀ¶ČµÄ¹ż³ĢÖŠ£¬·¢ĻÖ2NO£Øg£©+O2 £Øg£© 2NO2 £Øg£©µÄ·“Ó¦ĖŁĀŹ±äĀż£¬½įŗĻøĆ·“Ó¦µÄĮ½²½·“Ó¦¹ż³Ģ·ÖĪöæÉÄܵÄŌŅņ£ŗ £Ø·“Ó¦Ī“Ź¹ÓĆ“ß»Æ¼Į£©”£
2NO2 £Øg£©µÄ·“Ó¦ĖŁĀŹ±äĀż£¬½įŗĻøĆ·“Ó¦µÄĮ½²½·“Ó¦¹ż³Ģ·ÖĪöæÉÄܵÄŌŅņ£ŗ £Ø·“Ó¦Ī“Ź¹ÓĆ“ß»Æ¼Į£©”£
£Ø4£©Čō£Ø2£©ÖŠ·“Ó¦ĢåĻµ£¬·“Ó¦æŖŹ¼Ź±Ź¹ÓĆ“ß»Æ¼Į£¬ĒėŌŚ£Ø2£©µÄĶ¼ÖŠ»³öøĆ·“Ó¦ĢåĻµ·“Ó¦½ų³ĢæÉÄܵÄĒśĻß”£
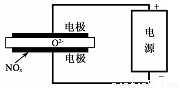
£Ø5£©µē½ā·Ø“¦ĄķµŖŃõ»ÆĪļŹĒÄæĒ°“óĘųĪŪČ¾ÖĪĄķµÄŅ»øöŠĀĖ¼Ā·”£ĘäŌĄķŹĒ½«NO£®ŌŚµē½ā³ŲÖŠ·Ö½ā³ÉĪŽĪŪČ¾µÄN2ŗĶ02³żČ„£¬ČēĶ¼ĖłŹ¾£¬£¬Į½µē¼«¼äŹĒ¹ĢĢåŃõ»ÆĪļµē½āÖŹ£¬ŌŚŅ»¶ØĢõ¼žĻĀæÉ×ŌÓÉ“«µ¼O2-”£Ōņµē½ā³ŲŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_____________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com