
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 2c(g);△H1<0
2c(g);△H1<0
x(g)+3y(g) 2z(g);△H2>0
2z(g);△H2>0
进行相关操作且达到平衡后(忽略体积改变所作的功),下列叙述错误的是
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
298K时,在20.0ml0.10mol/L氨水中滴入0.10mol/L的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol/L氨水的电离度为1.32%,下列有关叙述不正确的是
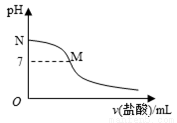
A.该滴定过程应该选择甲基橙作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)>c(H+)=c(OH-)
D.N点处的溶液中pH<13
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
25℃时,在浓度均为0.01mol/L的NaCN和HCN组成的混合溶液中,测得c(Na+)>c(CN-),则下列描述中不正确的是
A.该溶液的pH<7
B.CN-的水解程度大于HCN的电离程度
C.c(CN-)+c(HCN)=0.02 mol·L-1
D.c(CN-)+c(OH-)=0.01 mol·L-1+c(H+)
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。其中一种方法是还原沉淀法,该法的工艺流程为:
CrO42-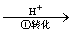 Cr2O72-
Cr2O72-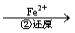 Cr3+
Cr3+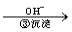 Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O。下列有关说法正确的是
Cr2O72-(橙色)+H2O。下列有关说法正确的是
A.第①步当2v(Cr2O72)=v(CrO42-)时,达到了平衡状态
B.对于上述平衡,加人适量稀硫酸后,溶液颜色变黄色,则有利于 CrO42-的生成
C.第②步中,还原 0.1molCr2O72-需要45.6gFeSO4
D.第③步沉淀剂a可以使用NaOH等碱性物质
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
容器 编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol/L FeCl3溶液:K+、NH4+、SCN-、NO3-
B.0.1mol/LCu(NO3)2溶液:Na+、Mg2+、Cl-、SO42-
C.0.5mol/L AlCl3溶液:K+、Na+、S2-、SO42-
D.由水电离产生的c(H+)=10-13 mol·L-1的溶液:K +、Na+、HCO3-、Cl-
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400 mL 0.01 mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是
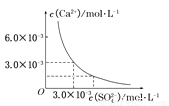
A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
已知草酸是二元弱酸,0.2mol/L NaHC2O4溶液显酸性,关于NaHC2O4溶液中离子浓度关系的叙述不正确的是
A.c(Na+)>c(HC2O4—)>c(C2O42—)>c(H2C2O4)
B.c(Na+)=c(HC2O4—)+c(C2O42—)+c(H2C2O4)
C.c(Na+)+c(H+)=c(HC2O4—)+c(C2O42—)+c(OH-)
D.c(H+)+c(H2C2O4)=c(C2O42—)+c(OH-)
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
室温时,M(OH)2(s) M2+(aq)+2OH-(aq) Ksp=a,c(M2+)="b" mol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq) Ksp=a,c(M2+)="b" mol·L-1时,溶液的pH等于
A.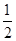 lg(
lg(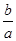 ) B.
) B.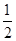 lg(
lg(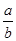 )
)
C.14+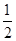 lg(
lg(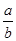 ) D.14+
) D.14+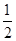 lg(
lg(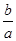 )
)
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,溶液呈血红色 | 待测液中含有Fe3+ |
B | 室温下,向浓度均为0.1 mol·L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀。 | Ksp(BaSO4)< Ksp(CaSO4) |
C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
D | 室温下,用pH试纸测得:0.1mol·L-1 Na2SO3溶液的pH约为10;0.1mol·L-1 NaHSO3溶液的pH约为5 | HSO3-结合H+的能力比SO32-的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com