
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+
HCOO-+H3O+
B.CO2+H2O HCO3-+H+
HCO3-+H+
C.CO32-+H2O HCO3-+OH-
HCO3-+OH-
D.HS-+H2O S2-+H3O+
S2-+H3O+
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
将0.1mol下列物质置于1L水中充分搅拌后,溶液中阴离子数最多的是
A.KCl B.Mg(OH)2 C .Na2CO3 D.MgSO4
.Na2CO3 D.MgSO4
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
在一定条件下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是10-amol/L和10-bmol/L,在此温度下,下列说法正确的是
A.a<b B.Kw=1.0×10-(7+ a) C.a=b D.Kw=1.0×10-(b+ a)
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
向三份0.1 mol·L-1NH4Cl溶液中分别加入少量Mg、NaOH、FeSO4固体(忽略溶液体积变化),则溶液中NH4+浓度的变化依次为
A.减小、增大、减小 B.减小、增大、增大
C.增大、减小、减小 D.减小、减小、增大[]
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
常温下,下列溶液的pH大于7的是
A.NH4Cl B.Al2(SO4)3 C.NaHCO3 D.Na2SO4
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,其中pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
A.HX、HZ、HY B.HY、HZ、HX C.HX、HY、HZ D.HZ、HY、HX
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:填空题
一定温度下,有①盐酸、②硫酸、③醋酸三种酸 (用①、②、③回答)。
(1)当其物质的量浓度相同时,c(H+)由大到小的顺序 ,pH由大到小的顺序是 ,取等体积的上述三种酸溶液,中和NaOH的能力由大到小的顺序是 。
(2)当c(H+)相同时,物质的量浓度由大到小的顺序为 ,取等体积的上述三种酸溶液,加入足量锌,产生的气体体积由大到小的顺序为 ,取等体积等浓度的NaOH溶液完全中和上述三种酸,所需酸溶液体积由大到小的顺序是 。
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:填空题
(1)某温度下重水(D2O)的离子积常数为1.6×10-15,像定义pH一样来规定pD=-lgc(D+),请回答以下问题:
①写出重水的电离方程式 。
②该温度下,重水中的pD=_____ ___(已知lg2=0.3)。
③0.01 mol/L的NaOD溶液中pD=____ ____。
(2)双氧水(H2O2)和水都是极弱电解质,但H2O2比水更显酸性。
①若把H2O2看成是二元弱酸,请写出它在水中第一步电离的方程式:______________。
②鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可以形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:_____________________。
③水电离生成H3O+ 和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离方程式为:_______________________。
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:填空题
根据题意,完成下列问题。
(1)常温下,将1 mL 0.05mol/L的H2SO4溶液加水稀释至100 mL,稀释后溶液的pH= 。若将pH=5的硫酸溶液稀释500倍,稀释后溶液中c(SO42-):c(H+)= 。
(2)某温度时,测得0.01mol•L-1的NaOH溶液的pH为11,该溶液与pH=5的HCl溶液等体积混合( 混合后溶液体积变化忽略不计),混合后溶液pH= 。
混合后溶液体积变化忽略不计),混合后溶液pH= 。
(3)常温下,pH=5的H2SO4溶液中由水电离出的H+的浓度为c1;pH=5的Al2(SO4)3溶液中由水电离出的H+的浓度为c2,溶液中 =_____________。
=_____________。
(4)常温下,pH=13的Ba(OH)2溶液aL与pH=3的H2SO4溶液bL混合(混合后溶液体积变化忽略不计),若所得混合溶液呈中性,则a :b=___________,若所得混合溶液pH=12,则a:b=___________。
查看答案和解析>>
科目: 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:实验题
某学生用0.10mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂。重复上述滴定操作2~3 次,记录数据如下。
(1)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A.滴定前平视读数,终点读数时仰视读数
B.锥形瓶水洗后未用待测盐酸润洗
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.标准液漏滴在锥形瓶外一滴
E.滴定前仰视读数 ,终点滴定后俯视读数
F.碱式滴定管尖嘴部分有气泡,滴定后消失
(2)若在达到滴定终点时,不慎多加了一滴NaOH溶液(一滴溶液体积约为0.05mL)继续加水到50 mL,所得溶液的pH为 。
(3)如图是向20mL的盐酸中逐渐加入0.1mol/L NaOH溶液时,溶液的pH变化图像,当滴加NaOH溶液为10mL时,该混合液的pH= ,(含lg表达式),若用该NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是 。
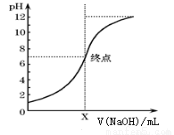
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(4)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:

①滴定时,滴定终点时滴定现象是_____________。
②该草酸溶液的物质的量浓度为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com